Einleitung: Einführung in das Atmungssystem
Halte für einen Moment die Luft an. Wie lange schaffst du das, während du diesen Text liest? Wahrscheinlich spürst du schon nach kurzer Zeit den drängenden, fast schmerzhaften Impuls, wieder einzuatmen. Dieser Impuls ist kein Zufall, sondern der wichtigste Überlebensmechanismus deines Körpers.

1. Das absolute Zeitlimit
Die Atmung ist der fundamentalste und zeitkritischste Prozess des menschlichen Körpers. Ein durchschnittlicher Mensch kann Wochen ohne Nahrung auskommen und Tage ohne Wasser überleben. Ohne Atmung (und damit ohne Sauerstoff) beginnen die ersten Gehirnzellen jedoch bereits nach etwa 3 Minuten unwiderruflich abzusterben.
2. Der Grund für die Atmung (Die Zellatmung)
Warum sind wir so extrem von diesem ständigen Luftstrom abhängig? Die Antwort liegt nicht in der Lunge, sondern auf mikroskopischer Ebene in jeder einzelnen Körperzelle.
- Energieproduktion: Jede Zelle benötigt Energie, um zu funktionieren und am Leben zu bleiben. Diese Energie wird in Form von Adenosintriphosphat (ATP) hergestellt.
- Der oxidative Prozess: Um dieses lebenswichtige ATP in ausreichender Menge zu produzieren, müssen die Zellen Nährstoffe verbrennen (oxidative Phosphorylierung). Für diese Verbrennung ist frischer Sauerstoff als Reaktionspartner absolut zwingend erforderlich.
- Die Müllabfuhr: Wo etwas verbrannt wird, entstehen Abgase. Bei der Zellatmung fällt unweigerlich Kohlendioxid als toxisches Abfallprodukt an.
3. Die doppelte Hauptaufgabe
Das respiratorische System hat folglich genau 2 Hauptaufgaben, die es pausenlos und zeitgleich erfüllen muss: Es muss den Sauerstoff aus der Umgebungsluft in den Körper holen und an das Blut übergeben. Gleichzeitig muss es das vom Blut antransportierte, giftige Kohlendioxid aus den Zellen aufnehmen und aus dem Körper ablüften.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Anatomie der oberen Atemwege
Die oberen Atemwege umfassen alle Strukturen vom Eintritt der Luft bis zum Kehlkopf. Ihre Hauptaufgabe ist die Reinigung, Befeuchtung und Erwärmung der Atemluft, bevor diese die empfindlichen Lungenbläschen erreicht.

1. Die Nase und Nasenhöhle (Die Klimaanlage)
Die Luft tritt primär durch die äußeren Nasenlöcher in den Vorhof der Nase ein.
- Filterfunktion: Grobe Haare im Nasenvorhof halten große Partikel wie Staub oder Insekten zurück.
- Die Conchae (Nasenmuscheln): Die Nasenhöhle ist durch 3 knöcherne Ausläufer – die obere, mittlere und untere Nasenmuschel – unterteilt. Diese Strukturen versetzen die einströmende Luft in starke Turbulenzen. Dadurch kommt die Luft länger mit der warmen, feuchten Schleimhaut in Kontakt.
- Schleimhaut und Epithel: Die Nasenhöhle ist mit respiratorischem Epithel ausgekleidet. Becherzellen produzieren Schleim, der kleinste Partikel einfängt, während Flimmerhärchen (Zilien) diesen Schleim kontinuierlich in Richtung Rachen befördern.
2. Der Pharynx (Rachen)
Der Rachen ist ein muskulöser Schlauch, der als gemeinsamer Weg für Luft und Nahrung dient. Er wird in genau 3 Abschnitte unterteilt.
- Nasopharynx: Er liegt hinter der Nasenhöhle und dient ausschließlich der Luftleitung. Hier mündet auch die Eustachische Röhre zum Druckausgleich des Ohres.
- Oropharynx: Dieser mittlere Teil hinter der Mundhöhle leitet sowohl Luft als auch Nahrung. Er ist mit einem robusteren, mehrschichtigen Plattenepithel ausgekleidet, um der Reibung beim Schlucken standzuhalten.
- Laryngopharynx: Der unterste Teil teilt sich schließlich in den vorderen Weg (Kehlkopf/Atemwege) und den hinteren Weg (Speiseröhre) auf.
3. Der Larynx (Kehlkopf)
Der Kehlkopf ist eine komplexe Struktur aus Knorpeln, die den Übergang zu den unteren Atemwegen bildet und das Herzstück der Stimmbildung darstellt.
- Die Knorpelstruktur: Er wird primär durch den großen Schildknorpel (Adamapfel) und den darunter liegenden Ringknorpel stabilisiert.
- Die Epiglottis (Kehldeckel): Dies ist ein sehr flexibler, blattförmiger Knorpel. Beim Schlucken legt sich die Epiglottis wie ein Schutzdeckel über den Eingang der Luftröhre (Glottis). Das stellt sicher, dass Nahrung und Flüssigkeit in die Speiseröhre geleitet werden und nicht in die Lunge gelangen.
- Die Stimmbänder (Vocal Folds): Im Inneren des Larynx befinden sich die paarigen Stimmlippen. Durch Muskelzug wird ihre Spannung verändert. Wenn Luft hindurchströmt, geraten sie in Schwingung und erzeugen Töne. Der Raum zwischen den Stimmbändern wird als Stimmritze (Glottis) bezeichnet.
💡 MERKE:
Die Nasenmuscheln erzeugen Turbulenzen zur Erwärmung der Luft. Der Pharynx besteht aus 3 Teilen: Naso-, Oro- und Laryngopharynx. Die Epiglottis ist der mechanische Wächter, der die Atemwege beim Schlucken verschließt. Die Glottis ist die engste Stelle der oberen Atemwege – ein kritischer Punkt bei Schwellungen!
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Anatomie der unteren Atemwege
Die unteren Atemwege beginnen exakt unterhalb des Kehlkopfs. Sie formen ein weitverzweigtes Röhrensystem, das in seiner Struktur oft als "auf dem Kopf stehender Baum" (Bronchialbaum) beschrieben wird.

1. Die Trachea (Luftröhre)
Die Trachea ist ein gerades, stabiles Rohr, das die Luft vom Kehlkopf bis zur Aufzweigung in die Lungenflügel leitet.
- Die Knorpelspangen: Um zu verhindern, dass die Luftröhre beim Einatmen durch den entstehenden Unterdruck in sich zusammenfällt, wird sie durch 16 bis 20 C-förmige Ringe aus hyalinem Knorpel offengehalten.
- Die flexible Rückwand: Diese Knorpelringe sind nicht komplett geschlossen. Die Rückseite der Luftröhre besteht aus einer weichen, muskulären Membran (Musculus trachealis). Der geniale Sinn dahinter: Direkt hinter der Luftröhre verläuft die Speiseröhre. Wenn du einen großen Bissen schluckst, kann sich die Speiseröhre in diese weiche Rückwand der Luftröhre ausdehnen, ohne blockiert zu werden.
- Die Carina: Am unteren Ende teilt sich die Luftröhre an einem Knorpelkamm namens Carina. Diese Stelle ist massiv mit Nervenenden durchsetzt. Wenn ein Fremdkörper (oder dein Absaugkatheter) diese Stelle berührt, löst das einen extremen, unkontrollierbaren Hustenreiz aus.
2. Die Bronchien und Bronchiolen (Das Leitungsnetz)
An der Carina teilt sich der Weg in exakt 2 Hauptbronchien auf, die in den rechten und linken Lungenflügel führen.
- Die anatomische Asymmetrie: Der rechte Hauptbronchus ist weiter, kürzer und verläuft deutlich steiler nach unten als der linke Hauptbronchus.
- Die Verzweigung: Die Hauptbronchien verästeln sich immer weiter in Lappenbronchien, dann in Segmentbronchien und schließlich in winzige Bronchiolen. Je weiter sich das System verzweigt, desto mehr nimmt der stützende Knorpel ab.
- Die Bronchiolen (Widerstandsgefäße): Diese Röhrchen haben einen Durchmesser von unter 1 Millimeter und besitzen absolut keinen Knorpel mehr. Ihre Wände bestehen fast vollständig aus glatter Muskulatur. Das parasympathische und sympathische Nervensystem kann diese Röhrchen verengen (Bronchokonstriktion) oder weiten (Bronchodilatation). Hier entfalten deine Inhalations-Medikamente (wie Salbutamol) ihre lebensrettende Wirkung.
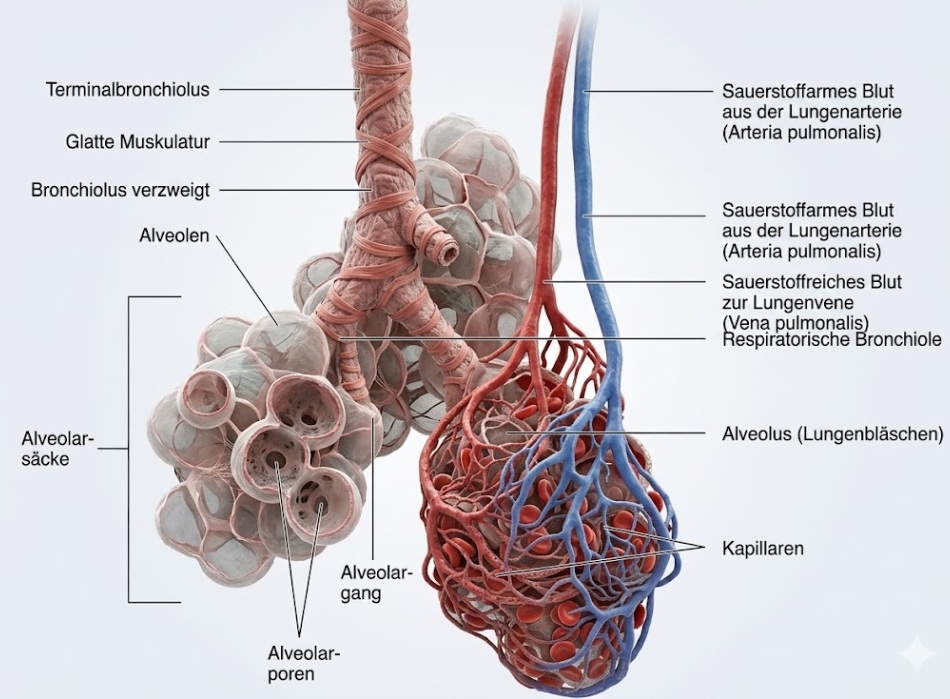
3. Die Alveolen (Die respiratorische Zone)
Ganz am Ende der feinsten Bronchiolen sitzen traubenförmige Säckchen – die Alveolen (Lungenbläschen). Sie haben einen Durchmesser von etwa 200 Mikrometer und sind der einzige Ort im Körper, an dem der Gasaustausch stattfindet.
- Typ-1-Alveolarzellen: Diese extrem dünnen Plattenepithelzellen bilden die eigentliche Wand der Bläschen. Zusammen mit der Wand der anliegenden Blutkapillare bilden sie die respiratorische Membran. Diese Membran ist nur etwa 0.5 Mikrometer dick – eine Barriere, die Sauerstoffmoleküle mühelos durchdringen können.
- Typ-2-Alveolarzellen (Surfactant): Da die feuchte Innenfläche der Alveolen eine hohe Oberflächenspannung besitzt, würden sie beim Ausatmen unweigerlich in sich zusammenfallen (kollabieren). Die Typ-2-Zellen produzieren daher "Surfactant" – eine seifenartige Substanz, welche die Oberflächenspannung massiv herabsetzt und die Lunge offen hält.
- Alveolarmakrophagen (Müllabfuhr): Da die Alveolen eine Sackgasse sind, patrouillieren hier spezielle Fresszellen (Makrophagen). Sie schlucken Staub, Bakterien und Fremdpartikel, die es bis hierhin geschafft haben.
💡 MERKE:
Die Trachea wird durch C-förmige Knorpelspangen offengehalten, ihre weiche Rückwand grenzt an die Speiseröhre. Die Carina ist der sensibelste Punkt für den Hustenreflex. Bronchiolen haben keinen Knorpel mehr, sondern glatte Muskulatur zur Steuerung des Luftstroms. In den Alveolen verhindert der Surfactant den lebensgefährlichen Kollaps der winzigen Bläschen.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Anatomie und Aufbau der Lunge
Die Lunge besteht aus exakt 2 kegelförmigen Organen, die durch das Mediastinum (den Raum mit dem Herzen) voneinander getrennt sind. Sie sind elastisch und haben eine schwammartige Textur.

1. Die makroskopische Gliederung
Obwohl wir von „der Lunge“ sprechen, sind der rechte und der linke Lungenflügel aufgrund der Lage des Herzens unterschiedlich aufgebaut.
- Der rechte Lungenflügel: Er ist etwas kürzer und breiter als der linke, da die Leber von unten dagegen drückt. Er ist in genau 3 Lappen unterteilt: den Oberlappen, den Mittellappen und den Unterlappen. Diese Lappen sind durch 2 tiefe Einschnitte (Fissuren) voneinander getrennt.
- Der linke Lungenflügel: Da das Herz leicht nach links geneigt ist, besitzt der linke Lungenflügel eine deutliche Einbuchtung, die Herzkerbe (Incisura cardiaca). Er besteht aus nur 2 Lappen: dem Oberlappen und dem Unterlappen, die durch 1 schräge Fissur getrennt sind.
- Apex und Basis: Die abgerundete Spitze (Apex) der Lunge ragt bis über das Schlüsselbein hinaus. Die breite Unterseite (Basis) ruht direkt auf dem Zwerchfell (Diaphragma).
- Das Lungenhilum: An der Innenseite jedes Lungenflügels befindet sich eine zentrale Eintrittspforte, das Hilum. Hier treten die Hauptbronchien sowie die Lungenarterien und Lungenvenen in das Organ ein oder aus.
2. Die Pleura (Die Hüllen der Lunge)
Die Lunge besitzt keine eigene Muskulatur, um sich auszudehnen. Sie ist für ihre Bewegung auf eine physikalische Kopplung mit der Brustwand angewiesen, die durch den Herzbeutel-ähnlichen Aufbau der Pleura (Brustfell) ermöglicht wird.
- Pleura visceralis (Lungenfell): Diese innere Schicht ist fest mit der Oberfläche der Lunge verwachsen und zieht sogar in die Fissuren zwischen den Lappen hinein.
- Pleura parietalis (Rippenfell): Diese äußere Schicht kleidet die Innenseite des Brustkorbs, das Zwerchfell und das Mediastinum aus.
- Der Pleuraspalt: Zwischen diesen beiden Schichten liegt ein hauchdünner Spalt, der mit einer geringen Menge an seröser Flüssigkeit gefüllt ist. Diese Flüssigkeit reduziert die Reibung beim Atmen auf fast 0. Viel wichtiger ist jedoch der physikalische Effekt: Im Pleuraspalt herrscht ein Unterdruck. Da die Flüssigkeit nicht auseinandergezogen werden kann, klebt die Lunge wie mit einem nassen Glasplättchen an der Brustwand fest. Wenn sich der Brustkorb hebt, muss die Lunge zwangsläufig mitgehen.
💡 MERKE:
Die rechte Lunge hat 3 Lappen, die linke Lunge nur 2 (wegen des Herzens).Das Lungenhilum ist die zentrale „Anschlussstelle“ für Bronchien und Gefäße. Die Pleura besteht aus exakt 2 Blättern, die durch Unterdruck im Pleuraspalt mechanisch gekoppelt sind. Ohne diesen Unterdruck würde die Lunge aufgrund ihrer Eigenelastizität sofort wie ein alter Luftballon in sich zusammenfallen.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Die Atemmuskulatur und Hilfsmuskulatur
Die Bewegung der Luft basiert auf einem simplen physikalischen Gesetz (Boyle-Mariotte): Vergrößerst du das Volumen eines geschlossenen Raumes (des Brustkorbs), sinkt der Druck im Inneren, und Luft wird von außen eingesaugt. Verkleinerst du das Volumen, steigt der Druck, und die Luft wird herausgepresst.
1. Die Hauptatemmuskulatur (Die Ruhe-Atmung)
Im normalen, entspannten Zustand benötigt der Körper für die Atmung lediglich 2 Muskelgruppen. Die Einatmung (Inspiration) ist ein aktiver Prozess, während die Ausatmung (Exspiration) in Ruhe völlig passiv abläuft.
- Das Zwerchfell (Diaphragma): Das ist der absolute Hauptmuskel der Atmung. Es ist eine kuppelförmige Muskelplatte, die den Brustkorb vom Bauchraum trennt. Zieht sich das Zwerchfell zusammen, flacht es ab und bewegt sich nach unten. Dadurch wird der Brustkorb in der Längsachse massiv vergrößert. Das Zwerchfell leistet in Ruhe etwa 75 Prozent der gesamten Atemarbeit.
- Äußere Zwischenrippenmuskeln (Mm. intercostales externi): Diese Muskeln verlaufen schräg zwischen den Rippen. Wenn sie sich anspannen, ziehen sie die Rippen nach oben und außen (wie den Henkel eines Eimers). Das vergrößert den Brustkorb in der Breite und Tiefe.
- Die passive Ausatmung: Um normal auszuatmen, müssen Zwerchfell und Zwischenrippenmuskeln einfach nur erschlaffen. Die elastischen Fasern der Lunge und die Schwerkraft des Brustkorbs ziehen das Gewebe völlig automatisch in seine Ursprungsform zurück, wodurch die Luft hinausgepresst wird.
2. Die Einatemhilfsmuskulatur (Das Notfall-System)
Wenn die normale Atmung nicht mehr ausreicht (bei starker sportlicher Belastung, Asthma oder COPD), reicht die Kraft des Zwerchfells nicht mehr. Der Körper rekrutiert nun zusätzliche Muskeln, die normalerweise am Hals und Schultergürtel liegen, um den Brustkorb mit Gewalt nach oben zu reißen.
- Musculus sternocleidomastoideus (Kopfnicker): Dieser kräftige Muskel zieht vom Hinterkopf zum Schlüsselbein und Brustbein. Wenn der Kopf fixiert ist, hebt er den vorderen Brustkorb massiv an.
- Musculi scaleni (Treppenmuskeln): Diese Muskeln verlaufen von der Halswirbelsäule zu den oberen 2 Rippen und ziehen diese ebenfalls kräftig nach oben.
- Pectoralis-Gruppe (Brustmuskeln): Auch die großen und kleinen Brustmuskeln können mithelfen, den Brustkorb zu weiten, wenn die Arme fest aufgestützt werden.
3. Die Ausatemhilfsmuskulatur (Aktives Auspressen)
Bei bestimmten Krankheitsbildern (wie einem schweren Asthma-Anfall) verkrampfen die Bronchien. Die Luft geht zwar noch hinein, ist aber beim Ausatmen gefangen. Die passive Ausatmung reicht nicht mehr aus. Der Patient muss die Luft nun aktiv und mit enormem Kraftaufwand aus der Lunge pressen.
- Bauchmuskulatur: Das ist die stärkste Waffe bei der Ausatmung. Die geraden und schrägen Bauchmuskeln ziehen sich krampfartig zusammen. Dadurch wird der Druck im Bauchraum massiv erhöht, und die Bauchorgane werden wie ein Stempel von unten gegen das entspannte Zwerchfell gepresst, was die Luft aus der Lunge treibt.
- Innere Zwischenrippenmuskeln (Mm. intercostales interni): Sie verlaufen entgegengesetzt zu den äußeren Muskeln und ziehen die Rippen aktiv und kraftvoll nach unten, um den Brustkorb gewaltsam zu verkleinern.
💡 MERKE:
Die Einatmung in Ruhe ist aktiv (Zwerchfell geht nach unten), die Ausatmung in Ruhe ist passiv (Entspannung).Bei Atemnot (Dyspnoe) wird die Einatemhilfsmuskulatur (Hals- und Schultermuskeln) zugeschaltet. Bei chronischer Atemwegsverengung (Asthma/COPD) muss die Bauchmuskulatur die Luft aktiv hinauspressen.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Topografie der Pleura und des Pleuraspalts
Die Pleura ist eine dünne, spiegelglatte und seröse Haut, die eine abgeschlossene Höhle um jeden Lungenflügel bildet. Sie besteht aus exakt 2 Blättern, die am Lungenhilum (der Eintrittspforte der Gefäße) direkt ineinander übergehen.

1. Die beiden Pleurablätter
- Pleura visceralis (Lungenfell): Dieses innere Blatt bedeckt die gesamte Oberfläche der Lunge und ist untrennbar mit dem Lungengewebe verwachsen. Es zieht sogar tief in die Fissuren zwischen den einzelnen Lungenlappen hinein.
- Pleura parietalis (Rippenfell): Dieses äußere Blatt kleidet die gesamte Innenseite des Brustkorbs aus. Je nachdem, an welcher Struktur es anliegt, wird es topografisch in unterschiedliche Abschnitte unterteilt: die Pleura costalis (an den Rippen), die Pleura diaphragmatica (auf dem Zwerchfell), die Pleura mediastinalis (zum Herzraum hin) und die Cupula pleurae (die Pleura-Kuppel, die bis über das Schlüsselbein hinausragt).
2. Der Pleuraspalt (Cavitas pleuralis)
Zwischen diesen beiden Blättern befindet sich ein hauchdünner, kapillärer Spaltraum.
- Die Gleitschicht: Der Spalt ist mit etwa 5 bis 10 Milliliter seröser Flüssigkeit gefüllt. Diese Flüssigkeit sorgt dafür, dass die Lunge bei jeder Atembewegung völlig reibungsfrei an der Brustwand entlanggleiten kann.
- Der Unterdruck (Intrapleuraler Druck): Im Pleuraspalt herrscht ein physikalischer Unterdruck (negativer Druck) gegenüber der Außenluft. Dieser Druck liegt in Ruhe bei etwa minus 4 Millimeter Quecksilbersäule. Da die Flüssigkeit im Spalt nicht auseinanderziehbar ist, werden das Lungenfell und das Rippenfell wie durch einen Saugnapf zusammengehalten. Dieser Unterdruck ist die einzige Kraft, die die elastische Lunge daran hindert, sich wie ein schlaffer Luftballon in Richtung Lungenhilum zusammenzuziehen.
3. Die Reserveräume (Pleura-Recessus)
Die Lunge füllt die Pleurahöhle im Ruhezustand nicht überall komplett aus. Es entstehen topografische Taschen, die als Reserveräume für tiefe Atemzüge dienen.
- Recessus costodiaphragmaticus (Sinus phrenicocostalis): Dies ist der klinisch wichtigste Raum. Er liegt am tiefsten Punkt der Pleurahöhle, dort wo das Zwerchfell auf die Rippenwand trifft. Bei tiefer Einatmung dehnt sich die Lunge in diesen Raum hinein aus.
- Klinische Relevanz: Da dies der tiefste Punkt im Stehen und Sitzen ist, sammelt sich hier bei Entzündungen oder Herzinsuffizienz zuerst Flüssigkeit an (Pleuraleffusion). Im Röntgenbild oder Ultraschall verschwindet dann die scharfe Ecke dieses Sinus – ein klassisches Zeichen für Flüssigkeit in der Lunge.
💡 MERKE:
Die Pleura visceralis klebt auf der Lunge, die Pleura parietalis an der Wand. Der Pleuraspalt ist ein physikalischer Verschluss durch Unterdruck. Die Cupula pleurae (Kuppel) ragt über die erste Rippe hinaus – Vorsicht bei Verletzungen am Hals! Der Sinus phrenicocostalis ist der tiefste Punkt und dient als "Auffangbecken" für Flüssigkeit.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Atemmechanik und Druckverhältnisse
Die Bewegung der Luft zwischen der Atmosphäre und den Lungenbläschen (Alveolen) wird ausschließlich durch Druckgefälle gesteuert. Luft fließt immer vom Ort des höheren Drucks zum Ort des niedrigeren Drucks. Um dieses Gefälle zu erzeugen, manipuliert der Körper das Volumen des Brustkorbs.
1. Die Drücke im Thorax (Die Ausgangslage)
Um die Atemmechanik zu verstehen, müssen wir exakt 3 verschiedene Drücke definieren, die in der Physiologie gemessen werden.
- Der atmosphärische Druck: Das ist der Außendruck der Umgebungsluft. Auf Meereshöhe beträgt dieser etwa 760 Millimeter Quecksilbersäule. In der Medizin wird dieser Wert als Referenzpunkt (Nullpunkt) gesetzt.
- Der intrapulmonale Druck (Alveolardruck): Das ist der Druck direkt im Inneren der Lungenbläschen. Bei offener Stimmritze und angehaltenem Atem gleicht sich dieser Druck exakt dem atmosphärischen Druck an (er ist dann genau 0 Millimeter Quecksilbersäule).
- Der intrapleurale Druck: Das ist der Druck im winzigen Pleuraspalt zwischen Lungenfell und Rippenfell. Dieser Druck ist immer leicht negativ (ein Unterdruck). In Atemruhe liegt er bei etwa minus 4 Millimeter Quecksilbersäule. Dieser permanente Unterdruck zieht die Lunge nach außen und verhindert ihren Kollaps.
2. Die Inspiration (Die aktive Sogwirkung)
Die Einatmung ist ein aktiver, muskelgetriebener Prozess zur Erzeugung eines Unterdrucks.
- Die Volumenzunahme: Das Zwerchfell zieht sich zusammen und flacht ab (bewegt sich nach unten), gleichzeitig heben die äußeren Zwischenrippenmuskeln den Brustkorb an. Das Volumen des gesamten Thorax wird massiv vergrößert.
- Der Druckabfall: Da die Lunge über den Pleuraspalt an der Brustwand klebt, wird auch ihr Volumen vergrößert. Nach dem Boyle-Mariotte-Gesetz sinkt der Druck in einem Raum, wenn man ihn vergrößert. Der intrapleurale Druck fällt auf etwa minus 6 bis minus 8 Millimeter Quecksilbersäule ab.
- Der Lufteinstrom: Dadurch wird auch der intrapulmonale Druck in den Alveolen auseinandergezogen. Er fällt auf etwa minus 1 bis minus 2 Millimeter Quecksilbersäule unter den atmosphärischen Außendruck. Dieses Gefälle reicht aus: Die Außenluft wird förmlich in die Lunge gesaugt, bis der Druck wieder ausgeglichen ist.
3. Die Exspiration (Das passive Auspressen)
Die normale Ausatmung in Ruhe erfordert keinerlei Muskelkraft, sie ist ein rein passiver Rückstellvorgang.
- Die Volumenabnahme: Die Einatemmuskulatur erschlafft. Die extrem elastischen Fasern des Lungengewebes und der knöcherne Brustkorb federn automatisch in ihre ursprüngliche, kleinere Form zurück.
- Der Druckanstieg: Durch die physikalische Verkleinerung des Raumes werden die Luftmoleküle in den Alveolen zusammengequetscht. Der intrapulmonale Druck steigt auf etwa plus 1 bis plus 2 Millimeter Quecksilbersäule über den atmosphärischen Druck.
- Der Luftausstrom: Da der Druck in der Lunge nun höher ist als in der Außenwelt, strömt die Luft automatisch aus dem Körper hinaus, bis der Druck wieder bei 0 liegt und der nächste Zyklus beginnt.
💡 MERKE:
Einatmung: Volumen steigt -> Druck sinkt (auf ca. minus 1 Millimeter Quecksilbersäule) -> Luft strömt hinein. Ausatmung: Volumen sinkt -> Druck steigt (auf ca. plus 1 Millimeter Quecksilbersäule) -> Luft strömt heraus. Der intrapleurale Druck im Spalt bleibt immer im Unterdruckbereich, um den Lungenkollaps zu verhindern.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Lungenvolumina und Kapazitäten
Die Luftmengen, die eine Lunge aufnehmen und bewegen kann, werden in primäre Volumina (einzelne Messwerte) und Kapazitäten (die Summe aus mindestens 2 Volumina) unterteilt. Die Messung dieser Werte erfolgt klassischerweise durch die Spirometrie.
1. Die primären Lungenvolumina
Diese 4 Basiswerte beschreiben die absoluten Luftmengen in den verschiedenen Phasen der Atmung.
- Das Atemzugvolumen (Tidalvolumen): Dies ist die Menge an Luft, die bei einer ganz normalen, entspannten Ruheatmung pro Atemzug ein- und ausgeatmet wird. Bei einem gesunden Erwachsenen liegt dieser Wert bei etwa 500 Milliliter.
- Das inspiratorische Reservevolumen: Wenn du nach einer normalen Einatmung mit voller Kraft weiter einatmest, bis die Lunge maximal gefüllt ist, nutzt du diese Reserve. Sie umfasst gewaltige 3000 Milliliter.
- Das exspiratorische Reservevolumen: Wenn du nach einer normalen Ausatmung die restliche Luft mit Hilfe deiner Bauchpresse gewaltsam aus der Lunge drückst, bewegst du dieses Volumen. Es beträgt etwa 1200 Milliliter.
- Das Residualvolumen: Selbst wenn du mit allergrößter Anstrengung ausatmest, bekommst du die Lunge niemals komplett leer. Es bleiben immer etwa 1200 Milliliter Luft in der Lunge zurück. Dieses Volumen ist essenziell, da es die Alveolen offen hält und verhindert, dass die Lunge kollabiert.
2. Die Lungenkapazitäten (Die Summenwerte)
Durch die Addition der primären Volumina erhalten wir klinisch hochrelevante Kapazitäten.
- Die Vitalkapazität: Das ist das absolute Maximum an Luft, das du nach maximaler Einatmung mit einem einzigen, maximalen Atemzug wieder auspusten kannst (Atemzugvolumen plus beide Reservevolumina). Sie liegt bei etwa 4700 Milliliter.
- Die Totale Lungenkapazität: Das ist das absolute Gesamtvolumen der Lunge (Vitalkapazität plus Residualvolumen). Es beträgt bei einem durchschnittlichen Erwachsenen etwa 6000 Milliliter.
3. Der anatomische Totraum (Die Verlustzone)
Das ist für dich der wichtigste Faktor bei der Beatmung! Nicht jeder Milliliter Luft, den du einatmest, erreicht auch die Lungenbläschen (Alveolen), um am Gasaustausch teilzunehmen.
- Das Leitungssystem: Die Luftröhre und die Bronchien leiten die Luft nur, sie können keinen Sauerstoff ins Blut abgeben. Das Volumen dieses Röhrensystems wird als anatomischer Totraum bezeichnet und beträgt bei einem Erwachsenen konstant etwa 150 Milliliter.
- Die alveoläre Ventilation: Wenn du in Ruhe 500 Milliliter einatmest, bleiben 150 Milliliter im Totraum hängen. Nur 350 Milliliter erreichen die Alveolen. Die Formel für die effektive Atemluft lautet also immer: Atemzugvolumen minus Totraum.
💡 MERKE:
Das Atemzugvolumen in Ruhe beträgt 500 Milliliter. Die Vitalkapazität ist das maximal verschiebbare Volumen (ca. 4700 Milliliter).Das Residualvolumen (ca. 1200 Milliliter) verlässt die Lunge niemals. Der anatomische Totraum (ca. 150 Milliliter) nimmt nicht am Gasaustausch teil und verringert die effektive Alveolarluft massiv.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Gasaustausch an der Blut-Luft-Schranke
Der Gasaustausch zwischen der Lunge und dem Blut wird als äußere Atmung bezeichnet. Er findet ausschließlich an der Blut-Luft-Schranke statt und basiert auf dem Prinzip der Diffusion – dem Bestreben von Teilchen, sich gleichmäßig im Raum zu verteilen.
1. Die Blut-Luft-Schranke (Die Barriere)
Damit Gase physikalisch von der Luft in das Blut übertreten können, müssen sie eine anatomische Grenze überwinden. Diese Schranke ist ein absolutes Meisterwerk der Minimalisierung und besteht aus exakt 3 hauchdünnen Schichten.
- Das Alveolarepithel: Die Innenwand des Lungenbläschens, bestehend aus extrem flachen Typ-1-Zellen.
- Die verschmolzene Basalmembran: Eine dünne Gewebeschicht, welche die Lunge direkt mit dem Blutgefäß verklebt.
- Das Kapillarendothel: Die Zellwand des kleinsten Blutgefäßes.
- Die Dimension: Zusammengenommen ist diese Barriere unvorstellbare 0.5 Mikrometer dünn. Zum Vergleich: Das ist etwa 100 mal dünner als ein menschliches Haar. Durch diese extrem kurze Distanz können Gase in Bruchteilen von Sekunden hindurchdiffundieren.
2. Das Gesetz der Partialdrücke (Der Antrieb)
Luft ist ein Gemisch aus verschiedenen Gasen (Stickstoff, Sauerstoff, Kohlendioxid). Der Gesamtdruck der Luft setzt sich aus den Teildrücken all dieser einzelnen Gase zusammen. Diese Teildrücke nennt man Partialdrücke.
- Der physikalische Motor: Ein Gas bewegt sich immer und unweigerlich von einem Ort mit hohem Partialdruck zu einem Ort mit niedrigem Partialdruck, bis beide Seiten exakt ausgeglichen sind.
3. Der Gasaustausch in Zahlen (Die Übergabe)
Wenn das sauerstoffarme Blut aus der rechten Herzhälfte an den Alveolen ankommt, treffen dort drastisch unterschiedliche Partialdrücke aufeinander.
- Die Sauerstoff-Beladung: In der frischen Alveolarluft herrscht ein Sauerstoff-Partialdruck von etwa 104 Millimeter Quecksilbersäule. Das ankommende, verbrauchte Blut hat nur noch einen Druck von etwa 40 Millimeter Quecksilbersäule. Dieses enorme Gefälle presst den Sauerstoff förmlich durch die Blut-Luft-Schranke in das Blut, bis dieses ebenfalls einen Druck von fast 104 Millimeter Quecksilbersäule erreicht hat.
- Die Kohlendioxid-Entsorgung: Gleichzeitig bringt das verbrauchte Blut das giftige Kohlendioxid mit einem Partialdruck von 45 Millimeter Quecksilbersäule aus dem Körper heran. In der frischen Alveolarluft beträgt der Druck für Kohlendioxid nur etwa 40 Millimeter Quecksilbersäule. Auch hier greift die Physik: Das Kohlendioxid diffundiert sofort aus dem Blut in die Alveole, um abgeatmet zu werden.
💡 MERKE:
Die Blut-Luft-Schranke ist nur 0.5 Mikrometer dick, um eine rasante Diffusion zu ermöglichen. Gase strömen immer vom hohen Partialdruck zum niedrigen Partialdruck. Das Sauerstoff-Gefälle ist massiv: 104 (Lunge) zu 40 (Blut) Millimeter Quecksilbersäule. Das Kohlendioxid-Gefälle ist klein, aber ausreichend: 45 (Blut) zu 40 (Lunge) Millimeter Quecksilbersäule.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Regulation der Atmung
Das Atemzentrum befindet sich tief im Hirnstamm, genauer in der Medulla oblongata (verlängertes Mark) und der Brücke (Pons). Von hier aus werden die elektrischen Befehle über den Nervus phrenicus an das Zwerchfell gesendet. Doch wie entscheidet das Atemzentrum, wie schnell und wie tief wir atmen müssen? Es nutzt ein zweigleisiges Sensorsystem.
1. Zentrale Chemorezeptoren (Der primäre Antrieb)
Entgegen der Intuition vieler Anfänger ist Sauerstoffmangel nicht der primäre Grund, warum ein gesunder Mensch atmet. Unser Hauptantrieb ist die Entsorgung von giftigem Abgas.
- Der Standort: Diese Sensoren sitzen direkt im Gehirn (in der Medulla oblongata), baden im Nervenwasser (Liquor) und sind von der Blut-Hirn-Schranke umgeben.
- Der Messwert: Sie messen nicht den Sauerstoff! Sie reagieren extrem sensibel auf einen Anstieg des Kohlendioxids im Blut. Kohlendioxid durchdringt die Blut-Hirn-Schranke mühelos und reagiert im Nervenwasser zu Kohlensäure. Dadurch sinkt der pH-Wert (es wird sauer).
- Die Reaktion: Sobald das Gehirn diese Übersäuerung durch Kohlendioxid registriert, feuert das Atemzentrum sofort Signale ab, um die Atemfrequenz und Atemtiefe drastisch zu steigern. Das überschüssige Kohlendioxid wird "abgelüftet".
2. Periphere Chemorezeptoren (Das Backup-System)
Zusätzlich zu den Sensoren im Gehirn gibt es Messstationen direkt im Blutkreislauf, die als eine Art Notfall-Backup dienen.
- Der Standort: Diese Rezeptoren befinden sich an exakt 2 strategischen Orten: im Aortenbogen und in der Halsschlagader (Glomus caroticum).
- Der Messwert: Sie messen primär den gelösten Sauerstoff im arteriellen Blut.
- Die Trägheit: Bei einem gesunden Menschen reagieren diese Sensoren sehr träge. Sie schlagen erst dann massiv Alarm und zwingen das Atemzentrum zur Arbeit, wenn der Sauerstoff-Partialdruck drastisch abfällt (typischerweise auf unter 60 Millimeter Quecksilbersäule).
3. Der Hypoxie-Antrieb (Klinische Relevanz)
Für dich im Rettungsdienst wird dieses System bei Patienten mit schweren chronischen Lungenerkrankungen (wie COPD) hochbrisant.
- Die Desensibilisierung: Ein COPD-Patient kann Kohlendioxid dauerhaft schlecht abatmen. Der Kohlendioxid-Wert im Blut ist chronisch stark erhöht. Nach einiger Zeit gewöhnen sich die zentralen Chemorezeptoren im Gehirn an diesen hohen Wert und stumpfen ab. Der primäre Kohlendioxid-Atemantrieb fällt komplett aus.
- Der Notlauf: Um nicht zu ersticken, schaltet der Körper des Patienten auf den Hypoxie-Antrieb (Sauerstoffmangel-Antrieb) um. Fortan atmet dieser Patient nur noch, weil die peripheren Sensoren am Hals melden, dass sein Sauerstoffwert gefährlich niedrig ist.
💡 MERKE:
Gesunde Menschen atmen primär, weil der Kohlendioxid-Spiegel im Gehirn steigt (zentrale Rezeptoren).Die peripheren Rezeptoren (Hals/Aorta) reagieren primär auf Sauerstoffmangel, greifen aber erst bei sehr niedrigen Werten (unter 60 Millimeter Quecksilbersäule) massiv ein. COPD-Patienten atmen fast ausschließlich aufgrund von Sauerstoffmangel (Hypoxie-Antrieb), da ihr Gehirn gegen das Kohlendioxid abgestumpft ist.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Der Gastransport im Blut
Der Transport der Atemgase ist ein chemisches Meisterwerk, das fast vollständig von den roten Blutkörperchen (Erythrozyten) und ihrem Hauptbestandteil, dem Hämoglobin, übernommen wird.
1. Der Sauerstofftransport (Das Hämoglobin)
Da sich nur etwa 1 bis 2 Prozent des Sauerstoffs direkt im wässrigen Blutplasma lösen, müssen die restlichen 98 bis 99 Prozent chemisch gebunden werden.
- Das Transportmolekül: Jedes Hämoglobin-Molekül besitzt exakt 4 Eisen-Ionen, an die jeweils ein Sauerstoffmolekül andocken kann.
- Die Sauerstoff-Hämoglobin-Dissoziationskurve: Diese S-förmige Kurve beschreibt das Bindungsverhalten. In der Lunge (bei hohem Sauerstoff-Partialdruck) bindet Hämoglobin den Sauerstoff extrem fest und sättigt sich zu fast 100 Prozent. Im Körpergewebe, wo der Partialdruck niedriger ist, ändert das Hämoglobin seine Form und lässt den Sauerstoff bereitwillig los, damit dieser in die Zellen diffundieren kann.
2. Der Bohr-Effekt (Die intelligente Sauerstoffabgabe)
Das Hämoglobin ist kein dummer Transporter, es spürt, wo im Körper die meiste Arbeit verrichtet wird. Dieser Mechanismus rettet Leben, besonders bei körperlicher Belastung.
- Der Mechanismus: Wenn ein Muskel stark arbeitet, produziert er Kohlendioxid und Milchsäure. Dadurch sinkt der pH-Wert im lokalen Gewebe (es wird sauer), und die Temperatur steigt.
- Die Rechtsverschiebung: Diese saure Umgebung zwingt das Hämoglobin dazu, seine Bindung zum Sauerstoff massiv zu lockern (die Dissoziationskurve verschiebt sich nach rechts). Das bedeutet: Genau dort, wo das Gewebe durch harte Arbeit übersäuert ist, wirft das Hämoglobin seinen rettenden Sauerstoff viel schneller und in viel größeren Mengen ab als in ruhendem Gewebe.
3. Der Kohlendioxidtransport (Die 3 Wege)
Kohlendioxid ist nicht nur Abfall, es ist die wichtigste Säure deines Körpers. Wenn es aus den Zellen in das Blut übertritt, nutzt es für die Reise zurück zur Lunge exakt 3 verschiedene Wege.
- Gelöst im Plasma (Der kleine Teil): Etwa 7 bis 10 Prozent des Kohlendioxids lösen sich einfach direkt im wässrigen Blutplasma.
- Gebunden an Hämoglobin (Der mittlere Teil): Etwa 20 Prozent binden sich direkt an die Aminosäuren des Hämoglobins (nicht an das Eisen!). Diese Form nennt man Carbaminohämoglobin.
- Als Bicarbonat (Der Hauptweg): Etwa 70 Prozent nutzen einen genialen chemischen Trick. Das Kohlendioxid wandert in das rote Blutkörperchen. Dort zwingt das Enzym Carboanhydrase das Kohlendioxid dazu, sich mit Wasser zu Kohlensäure zu verbinden. Diese zerfällt sofort in Wasserstoff-Ionen und Bicarbonat. Das Bicarbonat wird aus der Zelle in das Blutplasma gepumpt, während im Austausch Chlorid in die Zelle strömt (der sogenannte Chlorid-Shift). In der Lunge läuft dieser ganze Prozess dann rückwärts ab, um das Kohlendioxid wieder abzuatmen.
4. Der Haldane-Effekt (Der CO2-Magnet)
Während der Bohr-Effekt die Sauerstoffabgabe steuert, steuert der Haldane-Effekt die Kohlendioxidaufnahme.
- Das Prinzip: Je weniger Sauerstoff an das Hämoglobin gebunden ist, desto leichter und bereitwilliger kann es Kohlendioxid aufnehmen.
- Der biologische Sinn: Wenn das rote Blutkörperchen im tiefsten Gewebe ankommt und seinen Sauerstoff abwirft, wird es automatisch zu einem extrem starken Magneten für das dort anfallende Kohlendioxid. Es entlädt die saubere Fracht und nimmt den Müll nahtlos auf.
💡 MERKE:
Der Bohr-Effekt besagt: Saures Milieu (niedriger pH-Wert) zwingt das Hämoglobin zur Sauerstoffabgabe. Kohlendioxid wird zu 70 Prozent als Bicarbonat (gesteuert durch die Carboanhydrase) transportiert. Beim Chlorid-Shift verlässt Bicarbonat die Zelle, und Chlorid rückt als Ladungsausgleich nach. Der Haldane-Effekt besagt: Sauerstoffarmes Hämoglobin ist ein besserer Kohlendioxid-Transporter.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Ventilation-Perfusion-Matching (Durchblutungsanpassung)
Für einen optimalen Gasaustausch müssen exakt 2 Parameter im perfekten Gleichgewicht stehen: Die Ventilation (die Belüftung der Alveolen) und die Perfusion (die Durchblutung der anliegenden Kapillaren). Dieses Gleichgewicht wird als V/Q-Verhältnis bezeichnet.
1. Das Problem der lokalen Blockade
Im Alltag kommt es ständig vor, dass einzelne Lungenbläschen (Alveolen) schlecht belüftet werden – zum Beispiel durch einen zähen Schleimpfropf bei einer Bronchitis oder durch einen verschluckten Fremdkörper.
- Der Druckabfall: Wenn keine frische Luft mehr in diese spezifische Alveole strömt, wird der dort noch vorhandene Sauerstoff rasch vom Blut aufgebraucht. Der Sauerstoff-Partialdruck in dieser blockierten Alveole sinkt rapide ab.
- Die Gefahr (Rechts-Links-Shunt): Würde das Blut nun weiterhin ungehindert an dieser leeren Alveole vorbeifließen, könnte es keinen Sauerstoff aufnehmen. Es würde dunkelrot und ungesättigt zurück in die linke Herzhälfte fließen und sich dort mit dem frischen Blut aus den gesunden Lungenbereichen vermischen, was den globalen Sauerstoffgehalt des Körpers massiv absenken würde.
2. Der Euler-Liljestrand-Mechanismus (Die paradoxe Reaktion)
Um diese lebensgefährliche Fehlsteuerung zu verhindern, nutzt die Lunge einen Reflex, der im restlichen Körper exakt umgekehrt funktioniert.
- Die Körper-Reaktion (Vasodilatation): Wenn in deinem Beinmuskel Sauerstoffmangel herrscht, weiten sich dort die Blutgefäße, um mehr Blut und damit mehr rettenden Sauerstoff heranzuschaffen.
- Die Lungen-Reaktion (Vasokonstriktion): In der Lunge ist das Blut nicht der Empfänger, sondern der Abholer. Wenn eine Alveole meldet, dass sie keinen Sauerstoff mehr anzubieten hat, reagiert die kleine Arteriole, die zu dieser Alveole führt, mit einem massiven Krampf. Sie zieht sich stark zusammen (hypoxische pulmonale Vasokonstriktion).
- Der biologische Sinn: Es macht schlichtweg keinen Sinn, leere Lastwagen zu einer Fabrik zu schicken, die nichts produziert. Durch das Verengen der Gefäße wird der Blutfluss zu der nutzlosen Alveole drastisch gedrosselt.
3. Die Umleitung (Das Matching)
Dieser Mechanismus blockiert nicht einfach nur das Blut, er lenkt es aktiv um.
- Der Weg des geringsten Widerstands: Da das Gefäß zur kranken Alveole nun extrem verengt ist, sucht sich das Blut physikalisch den Weg des geringsten Widerstands.
- Die Optimierung: Das Blut weicht auf die Gefäße der benachbarten, gesunden und exzellent belüfteten Alveolen aus. Genau dort wird das Blut nun maximal mit Sauerstoff beladen. Die Lunge passt also ihre Durchblutung (Perfusion) in Echtzeit und völlig autonom an die lokal vorhandene Belüftung (Ventilation) an.
💡 MERKE:
Das V/Q-Verhältnis beschreibt das Gleichgewicht aus Belüftung und Durchblutung. Die hypoxische pulmonale Vasokonstriktion ist ein Lungen-Schutzreflex: Kein Sauerstoff bedeutet Gefäßverengung. Durch diese Verengung wird das Blut automatisch zu den gesunden, belüfteten Alveolen umgeleitet. Dies verhindert, dass sauerstoffarmes Blut ungenutzt zum Herzen zurückfließt.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Die physikalischen Gasgesetze
Neben dem Boyle-Mariotte-Gesetz (welches das Verhältnis von Druck und Volumen für die Atemmechanik erklärt) regeln exakt 2 weitere Gesetze den unsichtbaren Übergang der Gase zwischen der Lunge und dem Blut.
1. Das Dalton-Gesetz (Das Gasgemisch)
Das Gesetz von John Dalton beschreibt das Verhalten von Gasen in einem Gemisch. Die Luft, die wir einatmen, ist kein einzelnes Element, sondern eine Mischung aus primär Stickstoff, Sauerstoff und Spurengasen.
- Das Prinzip der Summe: Das Dalton-Gesetz besagt, dass sich der Gesamtdruck eines Gasgemisches aus der exakten Summe der Partialdrücke (Teildrücke) aller beteiligten Einzelgase zusammensetzt. Jedes Gas in diesem Gemisch übt seinen eigenen Druck völlig unabhängig von den anderen Gasen aus.
- Das Rechenbeispiel: Auf Meereshöhe beträgt der atmosphärische Gesamtdruck etwa 760 Millimeter Quecksilbersäule. Unsere Atemluft besteht zu etwa 21 Prozent aus Sauerstoff. Nach Dalton berechnet sich der Sauerstoff-Partialdruck ganz einfach: 21 Prozent von 760 ergeben etwa 159 Millimeter Quecksilbersäule.
- Klinische Anwendung: Wenn dein Patient einen extremen Sauerstoffmangel hat, drehst du die Sauerstoffflasche auf und verabreichst ihm Luft mit 100 Prozent Sauerstoff. Dadurch verdrängst du den nutzlosen Stickstoff aus der Maske und erhöhst den Partialdruck des Sauerstoffs künstlich auf volle 760 Millimeter Quecksilbersäule. Dieses gigantische Gefälle presst den Sauerstoff dann mit brutaler physikalischer Kraft in die Lunge.
2. Das Henry-Gesetz (Die Löslichkeit)
Das Gesetz von William Henry beschreibt, was passiert, wenn ein Gas auf eine Flüssigkeit (wie dein Blutplasma) trifft und sich darin lösen soll.
- Die zwei Faktoren: Das Henry-Gesetz besagt, dass die Menge eines Gases, die sich in einer Flüssigkeit löst, von exakt 2 Faktoren abhängt: dem Partialdruck des Gases über der Flüssigkeit und dem spezifischen Löslichkeitskoeffizienten des Gases selbst.
- Der Druck-Faktor: Je höher der Druck ist, mit dem das Gas auf die Oberfläche der Flüssigkeit gepresst wird, desto mehr Gasmoleküle werden in die Flüssigkeit hineingedrückt.
- Der Löslichkeits-Faktor: Jedes Gas löst sich unterschiedlich gut in Wasser. Das ist für dich essenziell: Kohlendioxid hat eine extrem hohe Löslichkeit. Es löst sich etwa 20 Mal besser in Blutplasma und in den wässrigen Schichten der Alveolen als Sauerstoff. Sauerstoff hingegen ist sehr schlecht wasserlöslich, weshalb wir das Hämoglobin als chemischen Transporter so dringend benötigen.
- Klinische Anwendung: Das Henry-Gesetz ist der Grund für die tödliche Taucherkrankheit (Dekompressionskrankheit). Wenn ein Taucher tief unter Wasser ist, herrscht ein gigantischer Druck. Dadurch löst sich massenhaft Stickstoff aus der Atemluft in seinem Blut. Taucht er zu schnell auf, sinkt der Umgebungsdruck schlagartig. Das Blut kann den Stickstoff nach dem Henry-Gesetz nicht mehr halten, das Gas perlt aus (wie beim Öffnen einer geschüttelten Sprudelflasche) und bildet tödliche Embolien in den Blutgefäßen.
💡 MERKE:
Das Dalton-Gesetz besagt: Gesamtdruck = Summe aller Partialdrücke. 21 Prozent Sauerstoff erzeugen 21 Prozent des Drucks. Das Henry-Gesetz besagt: Gaslöslichkeit in einer Flüssigkeit steigt mit dem Druck und der Löslichkeit des Gases. Kohlendioxid ist etwa 20 Mal besser wasserlöslich als Sauerstoff.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Atemarbeit (Resistance und Compliance)
Die Atemmechanik basiert auf Druckunterschieden. Wie viel Kraft die Atemmuskulatur jedoch aufwenden muss, um diese Drücke zu erzeugen und die Luft zu bewegen, wird durch den Strömungswiderstand und die Dehnbarkeit des Gewebes bestimmt.
1. Die Resistance (Der Atemwegswiderstand)
Die Resistance beschreibt die reine physikalische Reibung, die die Luft überwinden muss, während sie durch die Röhren der Atemwege strömt.
- Der limitierende Faktor: Genauso wie bei den Blutgefäßen wird der Widerstand fast ausschließlich durch den Radius der Bronchiolen bestimmt. Eine Halbierung des Radius führt zu einer Ver-16-fachung des Widerstands.
- Das Problem bei der Ausatmung: Da die Atemwege nicht durch Knorpel gestützt sind, werden sie beim aktiven Ausatmen durch den steigenden Druck im Brustkorb leicht komprimiert. Bei Gesunden ist das kein Problem. Bei Asthmatikern (krampfende Muskulatur) oder bei COPD (Schleim und chronische Entzündung) ist der Radius ohnehin schon winzig. Beim Ausatmen klappen diese Röhrchen dann komplett zu.
- Der Kraftaufwand: Um die Luft durch einen hohen Widerstand zu pressen, muss die Atemmuskulatur massiv Überdruck erzeugen. Die Atemarbeit steigt dramatisch an.
2. Die Compliance (Die Dehnbarkeit)
Die Compliance beschreibt die mechanische Elastizität der Lunge und des knöchernen Brustkorbs. Sie gibt an, wie viel Volumen sich pro aufgewendeter Druckeinheit verändert.
- Hohe Compliance (Die ausgeleierte Lunge): Eine extrem hohe Dehnbarkeit klingt zunächst gut, ist aber krankhaft (typisch für ein Lungenemphysem). Die Lunge verliert ihre elastischen Fasern. Man bekommt die Luft zwar extrem leicht hinein (wie in eine ausgeleierte Plastiktüte), aber da die elastische Rückstellkraft fehlt, bekommt man sie ohne massive Muskelarbeit der Bauchpresse nicht mehr heraus.
- Geringe Compliance (Die steife Lunge): Dies ist der absolute Notfall auf der Intensivstation und im Rettungsdienst. Die Lunge wird steif und unnachgiebig. Das passiert bei Lungenfibrose (Vernarbung) oder einem Lungenödem (Wasser im Gewebe).
- Der Kraftaufwand: Um eine Lunge mit geringer Compliance auch nur um 500 Milliliter zu füllen, muss das Zwerchfell einen gigantischen Unterdruck erzeugen. Die Inspiration fühlt sich an, als würde man versuchen, einen dicken Autoreifen mit dem Mund aufzupusten.
- Der Surfactant-Faktor: Wie wir bereits gelernt haben, ist die Produktion von Surfactant essenziell, um die Oberflächenspannung in den Alveolen zu senken. Ein Mangel an Surfactant (wie beim Atemnotsyndrom von Frühgeborenen) vernichtet die Compliance fast vollständig.
💡 MERKE:
Die Resistance ist der Strömungswiderstand, primär bestimmt durch den Durchmesser der Bronchiolen. Die Compliance ist die Dehnbarkeit der Lunge und des Brustkorbs.Eine steife Lunge (geringe Compliance) macht die Einatmung extrem muskelzehrend. Verengte Röhren (hohe Resistance) machen vor allem die Ausatmung zum Kraftakt.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Fötale Anpassung und Lungenentwicklung
Vor dem ersten Schrei existiert das ungeborene Kind in einer völlig anderen physikalischen Welt. Die Lunge ist mit Fruchtwasser gefüllt und nimmt nicht am Gasaustausch teil. Die Sauerstoffversorgung wird komplett an die Mutter ausgelagert.
1. Fötales Hämoglobin (Der chemische Diebstahl)
Da die fetale Lunge nicht belüftet ist, muss der Fötus seinen gesamten Sauerstoff aus dem mütterlichen Blut in der Plazenta beziehen. Dort herrscht jedoch ein Problem: Der Sauerstoff-Partialdruck in der Plazenta ist relativ niedrig.
- Die Struktur: Fötales Hämoglobin unterscheidet sich in seinem molekularen Aufbau leicht vom erwachsenen Hämoglobin der Mutter.
- Die Affinität: Durch diesen minimalen Strukturunterschied besitzt das fötale Hämoglobin eine extrem viel stärkere Bindungskraft (Affinität) für Sauerstoff als das mütterliche Hämoglobin.
- Der Transfer: Wenn das Blut der Mutter und das Blut des Fötus in der Plazenta aneinander vorbeifließen, verhält sich das fötale Hämoglobin wie ein extrem starker Magnet. Es entreißt dem mütterlichen Hämoglobin den Sauerstoff geradezu physikalisch und zieht ihn über die Schranke in den fötalen Kreislauf.
2. Die embryonale Lungenentwicklung (Der Zeitplan)
Obwohl die Lunge erst bei der Geburt benötigt wird, dauert ihre Entwicklung fast die gesamte Schwangerschaft an und verläuft in kritischen Etappen.
- Woche 4: Das Atmungssystem beginnt als winzige Ausstülpung (Atemdivertikel) am embryonalen Vorderdarm.
- Woche 16: Die Atemwege haben sich verzweigt und alle großen Bronchien und Bronchiolen sind angelegt. Es gibt jedoch noch keine Lungenbläschen (Alveolen) für den Gasaustausch. Ein Überleben außerhalb des Mutterleibs ist absolut unmöglich.
- Woche 20: Ein entscheidender Meilenstein! Die Typ-2-Alveolarzellen beginnen, sich zu differenzieren und produzieren die allerersten, winzigen Mengen an Surfactant (der rettenden Seifenlösung gegen den Lungenkollaps). Zudem beginnt der Fötus mit "Atembewegungen", um die Atemmuskulatur zu trainieren und Fruchtwasser in die Lunge zu ziehen.
- Woche 28: Ab diesem Zeitpunkt sind in der Regel ausreichend Alveolen gebildet und genug Surfactant vorhanden, um einem Frühgeborenen eine realistische Überlebenschance zu bieten, auch wenn oft noch intensivmedizinische Hilfe nötig ist.
3. Respiratory Distress Syndrome (Das Frühchen-Problem)
Wenn ein Kind deutlich zu früh (beispielsweise in Woche 24 oder 26) geboren wird, leidet es fast immer an einem Atemnotsyndrom (Respiratory Distress Syndrome).
- Der Mechanismus: Der primäre Grund für dieses Syndrom ist der absolute Mangel an Surfactant. Wie wir in den vorherigen Modulen gelernt haben, verhindert Surfactant, dass die Alveolen beim Ausatmen durch die hohe Oberflächenspannung des Wassers in sich zusammenfallen.
- Der Erschöpfungstod: Ohne Surfactant kollabiert die winzige Lunge des Frühchens nach jedem einzelnen Atemzug komplett. Um sie beim nächsten Atemzug wieder zu entfalten, muss das Baby eine gigantische Kraft aufwenden (die Compliance ist fast bei 0). Diese enorme Atemarbeit erschöpft das Frühchen innerhalb kürzester Zeit. Der Sauerstoffgehalt sinkt rapide, während der Kohlendioxid-Spiegel lebensgefährlich ansteigt.
- Die rettende Therapie: In der Klinik (oder durch den Notarzt) erhalten diese Kinder oft künstlichen Surfactant direkt über einen Beatmungsschlauch in die Lunge. Im Rettungswagen ist die sofortige Anwendung von Überdruckbeatmung (CPAP) entscheidend, um die Lunge mechanisch offenzuhalten.
💡 MERKE:
Fötales Hämoglobin bindet Sauerstoff deutlich stärker als erwachsenes Hämoglobin, um ihn der Mutter in der Plazenta zu entziehen. Die rettende Surfactant-Produktion beginnt um Woche 20, ist aber meist erst um Woche 28 ausreichend für eine problemlose Eigenatmung. Ein Frühgeborenes ohne Surfactant (Respiratory Distress Syndrome) leidet unter massiv kollabierenden Alveolen und stirbt unbehandelt an Erschöpfung und Sauerstoffmangel.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
