Einleitung: Einführung in das Herz-Kreislauf-System
Der menschliche Körper benötigt ein leistungsstarkes und unermüdliches Transportsystem, um zu überleben. Das kardiovaskuläre System, umgangssprachlich als Herz-Kreislauf-System bezeichnet, übernimmt genau diese lebenswichtige Aufgabe. Es versorgt das Körpergewebe kontinuierlich mit lebensnotwendigem Sauerstoff, essenziellen Nährstoffen und Hormonen. Gleichzeitig stellt es sicher, dass schädliche Stoffwechsel-Endprodukte wie Kohlendioxid rasch abtransportiert werden. Dieses geschlossene System besteht aus exakt 2 funktionellen Hauptkomponenten: der zentralen Pumpe und dem weitverzweigten Röhrensystem.
1. Das Herz (Die zentrale Pumpe)
Das Herz ist das unermüdliche Kraftwerk des Körpers. Es gibt absolut kein passenderes Wort für die Funktion dieses Organs als „Pumpe“, denn seine rhythmischen Kontraktionen erzeugen den notwendigen Druck, um das Blut mit enormer Kraft in die großen Blutgefäße – die Aorta und den Lungenstamm – auszuwerfen. Obwohl der Begriff der Pumpe oft an eine mechanische Maschine aus Stahl und Plastik erinnert, handelt es sich beim Herzen um ein hochkomplexes, muskuläres Organ, das sich dynamisch an die körperlichen Bedürfnisse anpasst. Von diesen großen Auswurfgefäßen ausgehend wird das Blut in den restlichen Körper verteilt.
2. Die Blutgefäße (Das logistische Netzwerk)
Während das Herz den Druck erzeugt, bilden die Blutgefäße die physischen Transportwege. Dieser vaskuläre Teil des Systems besteht aus Röhren unterschiedlicher Größe, die das Blut durch den gesamten Körper leiten. Neben dem reinen Transport bieten die feinsten Blutgefäße (die Kapillaren) den tatsächlichen physischen Ort, an dem der Gasaustausch und die Nährstoffübergabe mit den Körperzellen stattfinden. Wenn die Funktion dieser Gefäße reduziert oder blockiert ist, wird das dahinterliegende Gewebe sofort von der lebensrettenden Versorgung abgeschnitten, was zu massiven Gewebeschäden führt.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Lage und Aufbau des Herzens

1. Die Lage im Brustkorb (Das Mediastinum)
Das Herz ist ein muskulöses Organ, das massiv geschützt im Zentrum deines Brustkorbs liegt. Es befindet sich in einem speziellen zentralen Raum zwischen den beiden Lungenflügeln, der als Mediastinum bezeichnet wird.
- Die Ausrichtung: Das Herz liegt nicht exakt mittig wie ein Lot. Seine nach unten gerichtete Spitze (der Apex) ist leicht nach links geneigt, weshalb der linke Lungenflügel etwas kleiner ist, um dem Herzen Platz zu machen.
- Die Dimensionen: Bei einem Erwachsenen ist das Herz etwa so groß wie eine geschlossene Faust. Es misst etwa 12 Zentimeter in der Länge, 8 Zentimeter in der Breite und 6 Zentimeter in der Dicke.
2. Das Perikard (Der Herzbeutel)
Das Herz liegt nicht einfach frei in der Brusthöhle, sondern ist von einem mehrschichtigen, schützenden Sack umgeben – dem Perikard (Herzbeutel).
- Der fibröse Anteil: Die äußere Schicht (Pericardium fibrosum) besteht aus zähem, straffem Bindegewebe. Sie verankert das Herz sicher im Brustkorb und verhindert mechanisch, dass sich der Muskel bei einem massiven Bluteinstrom unkontrolliert überdehnt.
- Der seröse Anteil: Darunter liegt das innere, seröse Perikard, das aus exakt 2 feinen Blättern besteht. Das wandständige Blatt kleidet die Innenseite des festen Sacks aus, während das viszerale Blatt direkt auf dem Herzmuskel aufliegt.
- Die Perikardhöhle: Zwischen diesen beiden serösen Blättern befindet sich ein winziger Spalt, der mit einer geringen Menge an Schmierflüssigkeit gefüllt ist. Diese Flüssigkeit reduziert die Reibung bei jedem der Milliarden Herzschläge im Laufe eines Lebens auf ein absolutes Minimum.
3. Die Schichten der Herzwand
Wenn wir den Herzbeutel durchtrennen und direkt in den Herzmuskel schneiden, erkennen wir, dass die Wand des Organs aus genau 3 unterschiedlichen Gewebeschichten aufgebaut ist.
- Das Epikard (Außenschicht): Dies ist die äußerste Schicht der Herzwand und sie ist anatomisch identisch mit dem viszeralen Blatt des Herzbeutels. In dieser Schicht verlaufen die lebenswichtigen Herzkranzgefäße (Koronararterien), die den Herzmuskel selbst mit Sauerstoff versorgen.
- Das Myokard (Muskelschicht): Dies ist die mit Abstand dickste Schicht und der eigentliche Motor des Organs. Sie besteht aus dem speziellen, quergestreiften Herzmuskelgewebe. Da die linke Herzkammer das Blut gegen hohen Widerstand in den gesamten Körper pumpen muss, ist das Myokard auf der linken Seite massiv dicker als auf der rechten Seite, die das Blut lediglich in die benachbarte Lunge fördert.
- Das Endokard (Innenschicht): Dies ist eine hauchdünne, spiegelglatte Schicht aus einfachem Plattenepithel, die alle Innenräume des Herzens auskleidet und auch die Herzklappen überzieht. Diese spiegelglatte Oberfläche ist essenziell, damit das Blut ungehindert fließen kann und sich keine lebensgefährlichen Blutgerinnsel (Thromben) an der Herzwand bilden.

💡 MERKE:
Das Perikard ist der reibungsmindernde, schützende Beutel um das gesamte Organ. Das Epikard ist die äußerste Haut, in der die Herzkranzgefäße verlaufen. Das Myokard ist der kräftige Muskel, wobei die linke Seite für den Körperkreislauf extrem verdickt ist. Das Endokard ist die spiegelglatte Innenauskleidung zur Verhinderung von Blutgerinnseln.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Die Innenarchitektur des Herzens (Räume und Klappen)

1. Die Herzhöhlen (Vorhöfe und Kammern)
Das Herz ist im Inneren in exakt 4 separate Hohlräume unterteilt, die paarweise (als rechte und linke Herzhälfte) zusammenarbeiten. Jede Hälfte besteht aus einer Vor- und einer Hauptkammer.
- Rechter Vorhof (Atrium dextrum): Er dient als Sammelbecken für das sauerstoffarme, kohlendioxidreiche Blut, das aus dem gesamten Körper über die große Hohlvene zurückströmt.
- Rechte Herzkammer (Ventriculus dexter): Sie empfängt das Blut aus dem rechten Vorhof und pumpt es in den Lungenstamm (Truncus pulmonalis), damit es in der Lunge mit frischem Sauerstoff angereichert werden kann.
- Linker Vorhof (Atrium sinistrum): Hier sammelt sich das frisch mit Sauerstoff angereicherte Blut, das aus den Lungenvenen zurückkehrt.
- Linke Herzkammer (Ventriculus sinister): Dies ist die leistungsstärkste Kammer des Herzens. Sie pumpt das sauerstoffreiche Blut mit enormem Druck in die Hauptschlagader (Aorta) und damit in den gesamten Körperkreislauf.
2. Die Herzscheidewand (Das Septum)
Damit sich das sauerstoffarme Blut der rechten Seite niemals mit dem sauerstoffreichen Blut der linken Seite vermischt, sind die beiden Herzhälften durch eine muskuläre Wand strikt voneinander getrennt.
- Vorhofseptum: Dieser obere Teil der Wand trennt den rechten vom linken Vorhof.
- Kammerseptum: Dieser wesentlich dickere und kräftigere Teil der Wand trennt die beiden großen Hauptkammern voneinander ab.
3. Die Segelklappen (Atrioventrikularklappen)
Herzklappen funktionieren wie Einwegventile – sie stellen sicher, dass das Blut nicht zurückschwappt. Die Segelklappen befinden sich zwischen den Vorhöfen und den Kammern.
- Die Trikuspidalklappe: Sie liegt auf der rechten Seite zwischen Vorhof und Kammer. Wie der Name sagt, besteht sie aus 3 feinen, häutigen Segeln.
- Die Bikuspidalklappe (Mitralklappe): Sie liegt auf der linken Seite zwischen Vorhof und Kammer. Sie besteht aus nur 2 Segeln und erinnert in ihrer Form an die Kopfbedeckung eines Bischofs (eine Mitra).
4. Die Taschenklappen (Semilunarklappen)
Diese Klappen befinden sich an den Ausgängen der beiden Hauptkammern und verhindern, dass das in die großen Gefäße ausgeworfene Blut in der Entspannungsphase wieder in das Herz zurückfließt.
- Die Pulmonalklappe: Sie liegt zwischen der rechten Herzkammer und dem Lungenstamm. Sie besteht aus 3 halbmondförmigen Taschen, die sich mit Blut füllen und den Rückweg verschließen, sobald der Druck in der Kammer abfällt.
- Die Aortenklappe: Sie liegt zwischen der linken Herzkammer und der Aorta und funktioniert nach exakt demselben halbmondförmigen Taschen-Prinzip, muss dabei aber dem massiven Druck des Körperkreislaufs standhalten.
💡 MERKE:
Das Septum trennt das Herz in eine rechte (sauerstoffarme) und eine linke (sauerstoffreiche) Hälfte. Die Segelklappen (Trikuspidal rechts, Mitral links) trennen die Vorhöfe von den Kammern. Die Taschenklappen (Pulmonal rechts, Aortal links) sichern die großen Auswurfgefäße ab.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Die Gefäßversorgung des Herzens (Koronarkreislauf)
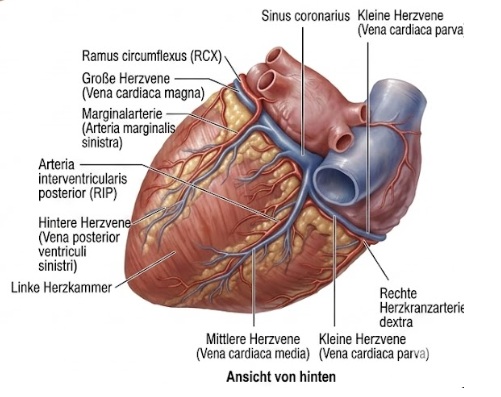

1. Die Koronararterien (Die Versorgungsleitungen)
Die Herzkranzgefäße entspringen direkt an der Basis der Hauptschlagader (Aorta), unmittelbar oberhalb der Aortenklappe, und verlaufen netzartig außen auf dem Herzmuskel im Epikard. Der Körper besitzt exakt 2 Hauptkoronararterien.
- Linke Koronararterie (LCA): Diese Arterie ist für das Überleben essenziell, da sie die massive linke Herzhälfte versorgt. Sie teilt sich kurz nach ihrem Ursprung in 2 gewaltige Äste auf: den Ramus circumflexus (RCX), der die Seiten- und Hinterwand versorgt, und den Ramus interventricularis anterior (RIVA), der die komplette Vorderwand der linken Kammer speist.
- Rechte Koronararterie (RCA): Diese Arterie verläuft in der Furche auf der rechten Seite. Sie versorgt den rechten Vorhof, die rechte Kammer sowie in den meisten Fällen essenzielle Teile des elektrischen Erregungsleitungssystems (wie den Sinus- und AV-Knoten).
2. Das physikalische Paradoxon (Die Diastolen-Durchblutung)
Der Koronarkreislauf weist eine physikalische Besonderheit auf, die ihn von jedem anderen Gefäßsystem im menschlichen Körper unterscheidet.
- Die Blockade in der Systole: Wenn sich der Herzmuskel anspannt, um das Blut auszuwerfen, übt er einen so enormen Druck auf sich selbst aus, dass die kleinen Blutgefäße im Muskelgewebe regelrecht zusammengequetscht werden. Der Blutfluss in das Myokard stoppt in diesem Moment.
- Die Füllung in der Diastole: Die eigentliche Durchblutung und Sauerstoffversorgung des Herzmuskels findet fast ausschließlich in der Entspannungsphase (Diastole) statt, wenn der Muskel erschlafft und der Weg für das Blut durch die Gefäße wieder frei ist.
3. Die Koronarvenen (Der Abtransport)
Nachdem das Blut seinen lebensrettenden Sauerstoff an die Zellen abgegeben hat, muss das nun kohlendioxidreiche Blut schnellstmöglich wieder abtransportiert werden.
- Das Venennetz: Parallel zu den Arterien verlaufen die Herzvenen, darunter die große Herzvene (Vena cordis magna), die mittlere und die kleine Herzvene.
- Der Sinus coronarius: All diese Venen sammeln sich auf der Rückseite des Herzens in einem großen, dünnwandigen Sammelrohr, dem Sinus coronarius.
- Der Rückfluss: Der Sinus coronarius mündet direkt in den rechten Vorhof. Dort mischt sich das verbrauchte Blut des Herzmuskels mit dem sauerstoffarmen Blut aus dem restlichen Körper, um gemeinsam den Weg in die Lunge anzutreten.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Aufbau des Gefäßsystems
Das Blutgefäßsystem bildet einen geschlossenen Kreislauf, der strukturell in 3 grundlegende Gefäßarten unterteilt wird: Arterien, Kapillaren und Venen. Grundsätzlich bestehen die Wände der größeren Gefäße (Arterien und Venen) aus 3 Gewebeschichten: der inneren Tunica intima (spiegelglattes Endothel), der mittleren Tunica media (glatte Muskulatur) und der äußeren Tunica externa (Bindegewebe). Die Ausprägung dieser Schichten variiert jedoch je nach Gefäßart extrem.

1. Arterien (Das Hochdrucksystem)
Arterien definieren sich unabhängig vom Sauerstoffgehalt immer dadurch, dass sie das Blut vom Herzen weg transportieren.
- Struktur für Druck: Da das Blut direkt aus der linken Herzkammer in die Arterien schießt, stehen diese Gefäße unter extremem Druck. Um nicht zu zerreißen, besitzen Arterien eine massiv verdickte Tunica media, die reich an glatter Muskulatur und elastischen Fasern ist.
- Windkesselfunktion: Die größten Arterien nahe dem Herzen (wie die Aorta) sind besonders elastisch. Sie dehnen sich beim Auswurf des Blutes wie ein Ballon und ziehen sich in der Erholungsphase des Herzens wieder zusammen. Das wandelt den stoßweisen Herzschlag in einen kontinuierlichen Blutfluss um.
- Widerstandsgefäße (Arteriolen): Die kleinsten Arterien besitzen fast nur noch Muskulatur. Sie können sich verengen oder weiten und sind damit die Hauptregulatoren deines Blutdrucks.
2. Kapillaren (Der Ort des Austauschs)
Die Arteriolen verzweigen sich schließlich in ein gigantisches, mikroskopisch kleines Netzwerk aus Haargefäßen – den Kapillaren. Hier findet die eigentliche Arbeit des Kreislaufs statt.
- Minimalistische Struktur: Kapillaren müssen Stoffe durchlassen. Daher besitzen sie weder eine Muskelschicht noch eine äußere Bindegewebshülle. Ihre Wand besteht aus exakt 1 einzigen Schicht von Endothelzellen.
- Der Stoffaustausch: Durch diese hauchdünne Barriere können Sauerstoff, Glukose und Wasser mühelos ins Gewebe diffundieren, während Kohlendioxid und Zellabfall in das Blut aufgenommen werden.
3. Venen (Das Niederdruck- und Speichersystem)
Venen definieren sich dadurch, dass sie das Blut zum Herzen hin transportieren. Nachdem das Blut das Kapillarbett durchquert hat, ist der vom Herzen erzeugte Blutdruck fast vollständig abgefallen.
- Dünnere Wände: Da in den Venen kaum noch Druck herrscht, ist ihre Muskelwand (Tunica media) im Vergleich zu den Arterien deutlich dünner. Dafür ist ihr innerer Durchmesser (das Lumen) wesentlich größer, weshalb sie als Blutspeicher dienen. Etwa 64 Prozent deines gesamten Blutes befinden sich im Ruhezustand in den Venen.
- Die Venenklappen: Da der Druck nicht mehr ausreicht, um das Blut (besonders aus den Beinen) gegen die Schwerkraft zurück zum Herzen zu drücken, besitzen die Venen spezielle Einwegventile: die Venenklappen.
- Die Muskelpumpe: Um das Blut nach oben zu befördern, sind die Venen auf die Hilfe der umliegenden Skelettmuskulatur angewiesen. Wenn du beim Gehen deine Beinmuskeln anspannst, quetschen diese die Venen zusammen und drücken das Blut von Klappe zu Klappe nach oben in Richtung Herz.
💡 MERKE:
Arterien: Führen vom Herzen weg. Sie haben dicke, muskulöse Wände, um dem hohen Blutdruck standzuhalten. Kapillaren: Der Ort des Gasaustauschs. Sie bestehen aus nur 1 Zellschicht, damit Stoffe hindurchpassen. Venen: Führen zum Herzen zurück. Sie haben dünne Wände, ein weites Lumen als Blutspeicher und besitzen Venenklappen, die mit der Muskelpumpe zusammenarbeiten, um den Rückfluss gegen die Schwerkraft zu sichern.
Einleitung: Detaillierte Histologie der Blutgefäße
1. Die mikroskopischen Wandschichten (Die 3 Tunicae)
Mit Ausnahme der winzigen Kapillaren bestehen die Wände aller Blutgefäße aus exakt 3 Gewebeschichten, deren Ausprägung die Funktion des Gefäßes bestimmt.
- Tunica intima (Die Innenschicht): Dies ist eine hauchdünne Auskleidung aus Endothelzellen, die direkt mit dem Blut in Kontakt steht. Sie muss spiegelglatt sein, um Reibung zu minimieren. Bei größeren Arterien ist diese Schicht zusätzlich mit einer inneren elastischen Membran unterlegt, die wie ein Gummiband wirkt.
- Tunica media (Die Mittelschicht): Dies ist die Arbeitsmuskulatur des Gefäßes, bestehend aus ringförmig angeordneter glatter Muskulatur und elastischen Fasern. Gesteuert durch das Nervensystem kann sich diese Schicht zusammenziehen (Vasokonstriktion) oder entspannen (Vasodilatation), was den Blutfluss und den Blutdruck massiv verändert.
- Tunica externa (Die Außenschicht): Dies ist eine robuste Hülle aus Kollagenfasern, die das Gefäß vor dem Zerreißen schützt und es im umliegenden Gewebe verankert. Eine faszinierende Besonderheit: Große Gefäße wie die Aorta sind so dick, dass ihre äußeren Wandschichten nicht mehr vom Blut im Inneren ernährt werden können. Sie besitzen daher ein eigenes Netzwerk an winzigen Blutgefäßen in der Außenwand – die Vasa vasorum („Gefäße der Gefäße“).
2. Die Sub-Typen der Arterien
Nicht jede Arterie ist gleich gebaut. Wenn wir uns vom Herzen wegbewegen, verändert sich ihre Struktur dramatisch.
- Elastische Arterien: Dies sind die größten Gefäße direkt am Herzen (wie die Aorta oder der Lungenstamm). Ihre Wände enthalten Unmengen an elastischen Fasern, um die enorme Druckwelle des Herzschlags wie ein Ballon abzufedern (Windkesselfunktion).
- Muskuläre Arterien: Weiter vom Herzen entfernt nimmt der elastische Anteil ab und der Anteil an glatter Muskulatur extrem zu. Dies sind die „Verteiler“, die das Blut gezielt zu spezifischen Organen lenken (wie die Arteria radialis am Arm).
- Arteriolen (Widerstandsgefäße): Das sind mikroskopisch kleine Arterien, deren Wände fast nur noch aus Muskulatur bestehen. Sie sind die absoluten Hauptregulatoren deines Blutdrucks. Durch ihr Engstellen erzeugen sie den wesentlichen peripheren Widerstand im Körperkreislauf.
3. Die 3 Arten von Kapillaren
Die Kapillaren bestehen nur noch aus einer einzigen Schicht Endothel (Tunica intima). Doch je nachdem, in welchem Organ sie sich befinden, lassen sie unterschiedlich viel Material durch ihre Wände.
- Kontinuierliche Kapillaren: Dies ist der Standardtyp, der in den meisten Geweben (wie Haut und Muskeln) vorkommt. Die Endothelzellen bilden eine fast lückenlose Röhre. Nur Wasser und sehr kleine Moleküle können durch winzige Spalten hindurchdiffundieren. Im Gehirn sind sie sogar so dicht verschweißt, dass sie die streng reglementierte Blut-Hirn-Schranke bilden.
- Fenestrierte Kapillaren: Diese Kapillaren besitzen richtige Poren (Fenestrae) in ihren Wänden. Sie finden sich dort, wo sehr viel Flüssigkeit und Nährstoffe schnell ausgetauscht werden müssen – zum Beispiel in den Dünndarmzotten oder den Filtern der Nieren.
- Sinusoide Kapillaren: Das ist das Extrem. Diese Kapillaren haben riesige Lücken in ihrer Wand und eine unvollständige Basalmembran. Sie sehen aus wie ein Schweizer Käse. Durch diese massiven Löcher können sogar ganze Zellen oder riesige Plasmaproteine hindurchschlüpfen. Sie finden sich in der Leber, der Milz und im Knochenmark.

4. Die Durchblutungssteuerung (Präkapillare Sphinkter)
Der Körper besitzt schlichtweg nicht genug Blutvolumen, um alle Kapillaren des Körpers gleichzeitig zu durchbluten.
- Ventilringe: Am Eingang jedes Kapillarbettes sitzen mikroskopisch kleine Muskelringe, die präkapillaren Sphinkter.
- Priorisierung: Wenn du gerade gegessen hast, öffnen sich die Sphinkter im Verdauungstrakt. Wenn du stattdessen plötzlich weglaufen musst, schließen sich diese Ventile im Bauchraum radikal und leiten das Blut stattdessen in die Kapillaren deiner Skelettmuskulatur um.
💡 MERKE:
Die Tunica media (Muskelschicht) steuert den Blutdruck durch Vasokonstriktion. Arteriolen sind die mikroskopischen Hauptregulatoren für den Gefäßwiderstand. Kapillaren haben 3 Durchlässigkeitsstufen: kontinuierlich (dicht), fenestriert (Poren) und sinusoid (riesige Löcher).Präkapillare Sphinkter leiten das Blut gezielt dorthin, wo es im Moment gebraucht wird.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Das Erregungsbildungs- und Leitungssystem
Das Herz besitzt die faszinierende Eigenschaft der Autorhythmie – es schlägt völlig selbstständig durch seine eigenen, im Herzen selbst generierten elektrischen Impulse. Diese elektrischen Vorgänge, von der Erzeugung bis zur Verteilung, lassen sich im EKG sichtbar machen.

1. Der Sinusknoten (Der primäre Schrittmacher)
Jede physiologische Herzaktion beginnt hoch oben im rechten Vorhof.
- Erregungsbildung: Der Sinusknoten ist der primäre Schrittmacher und der natürliche Taktgeber des Herzens.
- Frequenz: Er erzeugt in Ruhe eine Eigenfrequenz von 60 bis 100 elektrischen Impulsen pro Minute.
- Ausbreitung: Von hier aus breitet sich der elektrische Reiz wie eine Welle über die Muskulatur des rechten und linken Vorhofs aus, was zur Kontraktion der Vorhöfe führt.
2. Der AV-Knoten (Die Verzögerungsstation)
Nachdem die Vorhöfe erregt wurden, erreicht das Signal den Atrioventrikularknoten (AV-Knoten), der wie eine Mautstelle an der Grenze zwischen Vorhöfen und Kammern liegt.
- Die Zeitverzögerung: Der AV-Knoten leitet das Signal nicht sofort weiter, sondern bremst es gezielt für etwa 0.1 Sekunden ab.
- Der biologische Sinn: Diese kurze Verzögerung ist essenziell. Sie gibt den Vorhöfen die nötige Zeit, ihr Blut in die Kammern zu pumpen, bevor sich diese ihrerseits zusammenziehen.
- Sekundärer Schrittmacher: Fällt der Sinusknoten krankheitsbedingt aus, übernimmt der AV-Knoten als Ersatz die Reizbildung – allerdings mit einer deutlich langsameren Frequenz von nur noch 40 bis 50 Schlägen pro Minute.
3. His-Bündel und Tawara-Schenkel (Die Schnellstraßen)
Nach der Verzögerung muss der Impuls rasant in die riesigen Hauptkammern geleitet werden, um eine zeitgleiche Kontraktion zu gewährleisten.
- Das His-Bündel: Dieser kurze, aber entscheidende Abschnitt durchdringt das elektrisch isolierende Herzskelett, das die Vorhöfe von den Kammern trennt. Es fungiert als Tertiärschrittmacher und kann im absoluten Notfall eine Frequenz von 30 bis 40 Schlägen pro Minute generieren.
- Die Tawara-Schenkel: Das His-Bündel teilt sich im dicken Kammerseptum in einen rechten und einen linken Kammerschenkel auf. Diese leiten das Signal mit Höchstgeschwindigkeit in Richtung der Herzspitze.
4. Die Purkinje-Fasern (Die Endverteilung)
Ganz unten an der Herzspitze fächern sich die Schenkel auf.
- Erregung des Myokards: Diese feinen Purkinje-Fasern dringen in die Arbeitsmuskulatur ein und übertragen das elektrische Signal direkt auf die Muskelzellen der Herzkammern.
- Kontraktionsrichtung: Dadurch wird eine koordinierte Muskelkontraktion ausgelöst, die an der Herzspitze beginnt und das Blut kraftvoll nach oben zur Herzbasis in die großen Auswurfgefäße treibt.
5. Schutz und nervale Steuerung
- Refraktärzeit: Der Herzmuskel besitzt eine Schutzphase (Refraktärzeit), in der er nach einer Erregung nicht sofort wieder erregt werden kann. Dies verhindert ein elektrisches Chaos und schützt das Organ vor gefährlichen Taktstörungen.
- Die Modulation: Obwohl das Herz autonom arbeitet, wird es durch das vegetative Nervensystem gesteuert. Der Parasympathikus (Nervus vagus) senkt die Frequenz, die Schlagkraft und die Überleitungsgeschwindigkeit. Der Sympathikus hingegen wirkt als Gaspedal: Er steigert die Herzfrequenz, die Schlagkraft und die Reizleitung. Eine massive Überlastung durch den Sympathikus kann im schlimmsten Fall Extrasystolen, Tachykardien oder das lebensbedrohliche Kammerflimmern auslösen.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Die Herzmechanik (Der Herzzyklus)
Der Herzzyklus beschreibt die Abfolge aller mechanischen Ereignisse während eines einzigen Herzschlags. Die Steuerung erfolgt rein druckabhängig: Blut fließt immer vom Ort des höheren Drucks zum Ort des niedrigeren Drucks, wobei die Herzklappen als Rückschlagventile den Rückfluss verhindern.
1. Die Systole (Kontraktionsphase)
Die Systole dauert etwa 0.3 Sekunden und ist die Phase, in der das Blut aktiv aus den Kammern gepresst wird.
- Anspannungsphase (isovolumetrisch): Die Herzkammern sind maximal mit Blut gefüllt. Sobald die elektrische Erregung die Kammermuskulatur erreicht, beginnt diese sich zusammenzuziehen. Der Druck in den Kammern steigt schlagartig an und übersteigt sofort den Druck in den Vorhöfen, was zum Verschluss der Segelklappen führt (erster Herzton). Da der Druck in der Kammer jedoch noch niedriger ist als in der Aorta (etwa 80 Millimeter Quecksilbersäule), bleiben auch die Taschenklappen geschlossen. Das Volumen bleibt gleich (isovolumetrisch), während der Druck massiv ansteigt.
- Austreibungsphase: Sobald der Kammerdruck den Druck in den großen Gefäßen übersteigt (links etwa 80 Millimeter Quecksilbersäule, rechts etwa 10 Millimeter Quecksilbersäule), werden die Taschenklappen aufgestoßen. Das Blut schießt in den Kreislauf. Das Schlagvolumen beträgt etwa 70 Milliliter. In der linken Kammer erreicht der Druck einen Spitzenwert von etwa 120 Millimeter Quecksilbersäule.
2. Die Diastole (Entspannungsphase)
Die Diastole dauert etwa 0.5 Sekunden und dient der Erholung des Muskels sowie der erneuten Füllung der Kammern.
- Entspannungsphase (isovolumetrisch): Nach der Austreibung erschlafft das Myokard. Der Druck in den Kammern fällt rapide ab. Da der Druck in den großen Gefäßen nun wieder höher ist als in der Kammer, schlagen die Taschenklappen zu (zweiter Herzton). Alle 4 Klappen sind für einen Moment wieder geschlossen, das Volumen in der Kammer bleibt konstant niedrig.
- Füllungsphase: Fällt der Kammerdruck unter den Druck der Vorhöfe, öffnen sich die Segelklappen. Das Blut, das sich während der Systole in den Vorhöfen gestaut hat, fließt passiv in die Kammern (etwa 80 Prozent der Füllung). Am Ende der Diastole ziehen sich die Vorhöfe kurz zusammen, um die restlichen 20 Prozent des Blutes aktiv in die Kammern zu pressen. Damit ist die Kammer bereit für den nächsten Schlag.
3. Klinische Relevanz: Herztöne und Klappen
- Erster Herzton: Entsteht zu Beginn der Systole durch den Verschluss der Segelklappen und die Schwingung des Muskels (Anspannungston).
- Zweiter Herzton: Entsteht am Ende der Systole durch den Verschluss der Taschenklappen (Klappenton).
- Klappenfehler: Wenn Klappen nicht richtig schließen (Insuffizienz) oder verengt sind (Stenose), entstehen Turbulenzen im Blutfluss, die als Herzgeräusche zwischen oder während der Herztöne hörbar sind.
💡 MERKE:
Systole: Anspannungsphase (Klappen zu, Druck steigt) + Austreibungsphase (Taschenklappen auf, Blut raus).Diastole: Entspannungsphase (Klappen zu, Druck fällt) + Füllungsphase (Segelklappen auf, Blut rein).Das Schlagvolumen liegt bei etwa 70 Milliliter pro Kammer. Der Druck in der linken Kammer variiert zwischen etwa 0 und 120 Millimeter Quecksilbersäule.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Hämodynamik (Die Mathematik des Überlebens)
1. Das Herzminutenvolumen (Die globale Versorgung)
Das Herzminutenvolumen ist der absolut wichtigste Wert in der kardiovaskulären Physiologie. Es beschreibt die Menge an Blut, die von einer Herzkammer in exakt 1 Minute in den Kreislauf gepumpt wird.
- Die Formel: Das Herzminutenvolumen berechnet sich aus der Herzfrequenz multipliziert mit dem Schlagvolumen.
- Normwerte: In körperlicher Ruhe pumpt das Herz etwa 5 Liter pro Minute in den Körperkreislauf. Bei extremen sportlichen Belastungen kann das Herzminutenvolumen bei einem gesunden Menschen auf bis zu 20 Liter pro Minute ansteigen, bei Hochleistungssportlern sogar noch deutlich höher.
- Klinische Bedeutung: Fällt das Herzminutenvolumen ab, erhalten Gehirn, Nieren und andere lebenswichtige Organe nicht mehr genug Sauerstoff. Der Patient rutscht unweigerlich in einen lebensbedrohlichen Schockzustand.
2. Die Herzfrequenz (Der Taktgeber)
Die Herzfrequenz beschreibt die Anzahl der Herzschläge pro Minute. Sie wird primär durch den Sinusknoten vorgegeben.
- Normwerte: Ein gesunder Erwachsener hat in Ruhe eine Herzfrequenz von 60 bis 100 Schlägen pro Minute.
- Einflussfaktoren: Die Herzfrequenz wird durch das autonome Nervensystem gesteuert. Der Sympathikus (durch Adrenalin und Noradrenalin) beschleunigt den Herzschlag (positive Chronotropie). Der Parasympathikus bremst den Herzschlag ab (negative Chronotropie).
- Das Limit: Eine Steigerung der Herzfrequenz erhöht zunächst das Herzminutenvolumen. Steigt die Frequenz jedoch auf extreme Werte (zum Beispiel über 160 Schläge pro Minute), wird die Diastole (Entspannungsphase) so drastisch verkürzt, dass sich das Herz nicht mehr ausreichend mit Blut füllen kann. Das Herzminutenvolumen bricht dann plötzlich massiv ein.
3. Das Schlagvolumen (Die Pumpmenge)
Das Schlagvolumen ist die Menge an Blut, die bei einem einzigen Herzschlag aus der Herzkammer ausgeworfen wird. Es liegt in Ruhe bei etwa 70 Milliliter. Es berechnet sich aus der Differenz zwischen dem Füllungsvolumen vor der Systole (ca. 130 Milliliter) und dem Restblut, das nach der Systole in der Kammer verbleibt (ca. 60 Milliliter). Das Schlagvolumen wird durch exakt 3 Faktoren bestimmt, die für dich als Notfallsanitäter essenziell sind:
- Die Vorlast (Preload): Dies ist die Vordehnung der Herzmuskelfasern am Ende der Diastole, bedingt durch das einströmende Blutvolumen. Der Frank-Starling-Mechanismus besagt: Je mehr Blut in das Herz fließt und die Kammer dehnt, desto kräftiger zieht sich der Muskel beim nächsten Schlag zusammen. Ein hoher venöser Rückstrom erhöht also das Schlagvolumen.
- Die Kontraktilität (Inotropie): Dies ist die pure, muskuläre Schlagkraft des Herzens, völlig unabhängig von der Vorlast. Sie wird durch den Kalziumeinstrom in die Zellen bestimmt. Medikamente wie Adrenalin steigern die Kontraktilität massiv (positive Inotropie).
- Die Nachlast (Afterload): Dies ist der Widerstand, gegen den das Herz anpumpen muss, um die Taschenklappen aufzustoßen. Es ist im Wesentlichen der Blutdruck in der Aorta. Eine extrem hohe Nachlast (wie bei einer hypertensiven Krise) zwingt das Herz zu massiver Schwerstarbeit und senkt das ausgeworfene Schlagvolumen, wenn die Kontraktilität nicht gleichzeitig gesteigert wird.
💡 MERKE:
Herzminutenvolumen = Herzfrequenz x Schlagvolumen. Ein normales Ruhe-Herzminutenvolumen liegt bei etwa 5 Liter pro Minute. Eine extrem hohe Herzfrequenz senkt das Herzminutenvolumen, da die Füllungszeit fehlt. Das Schlagvolumen wird durch 3 Säulen definiert: Vorlast (Füllungsvolumen), Kontraktilität (Muskelkraft) und Nachlast (Gefäßwiderstand).
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Determinanten des Schlagvolumens
Das Schlagvolumen (die Menge an Blut, die pro Herzschlag ausgeworfen wird) ist keine feste Konstante. Es wird von Schlag zu Schlag dynamisch an die Bedürfnisse des Körpers angepasst. Diese Anpassung wird durch das komplexe Zusammenspiel von Vorlast, Nachlast und Kontraktilität gesteuert.
1. Die Vorlast (Preload)
Die Vorlast ist definiert als die Wandspannung der Herzkammern am absoluten Ende der Diastole (Entspannungsphase), unmittelbar bevor sich der Muskel zusammenzieht. Sie wird in der Praxis oft mit dem enddiastolischen Füllungsvolumen gleichgesetzt.
- Der Frank-Starling-Mechanismus: Dies ist ein physikalisches Gesetz des Herzmuskels. Je mehr Blut während der Diastole in die Herzkammer strömt, desto stärker werden die Muskelfasern gedehnt. Diese Vordehnung bringt die kontraktilen Proteine (Aktin und Myosin) in eine mechanisch optimale Position, wodurch sich der Muskel beim darauffolgenden Schlag deutlich kräftiger zusammenzieht.
- Das Limit: Dieser Mechanismus hat eine Grenze. Wird das Herz chronisch überdehnt (wie bei einer Herzinsuffizienz), reißen die Proteine quasi ab, die Pumpkraft bricht zusammen und das Blut staut sich rückwärts in die Lunge oder den Körper (Dekompensation).
- Klinische Anwendung: Wenn ein Patient durch eine Blutung massiv an Volumen verliert, sinkt der venöse Rückstrom und damit die Vorlast. Das Schlagvolumen bricht ein. Durch die schnelle Infusion von kristalloiden Lösungen (wie Ringer-Laktat) erhöhst du künstlich das Volumen, steigerst die Vorlast und nutzt den Frank-Starling-Mechanismus, um das Schlagvolumen und den Blutdruck wieder anzuheben. Medikamente wie Nitroglycerin bewirken genau das Gegenteil: Sie weiten die Venen, Blut versackt in den Beinen, die Vorlast sinkt und das Herz wird massiv entlastet.
2. Die Nachlast (Afterload)
Die Nachlast ist der mechanische Widerstand, den die Herzkammer überwinden muss, um die Taschenklappe aufzustoßen und das Blut in den Kreislauf auszuwerfen. Auf der linken Seite des Herzens entspricht die Nachlast primär dem Druck in der Aorta und dem peripheren Gefäßwiderstand.
- Die Wandspannung (Laplace-Gesetz): Je höher der Druck in der Aorta ist, desto mehr Wandspannung muss das Myokard aufbauen, um überhaupt erst die Klappe zu öffnen.
- Der fatale Effekt: Eine Erhöhung der Nachlast senkt das Schlagvolumen direkt. Das Herz muss einen Großteil seiner Energie aufwenden, um gegen die geschlossene Klappe anzudrücken, wodurch weniger Energie für den eigentlichen Auswurf übrig bleibt. Gleichzeitig steigt der Sauerstoffverbrauch des Herzmuskels extrem an.
- Klinische Anwendung: Bei einer hypertensiven Krise (Blutdruck zum Beispiel bei 220 Millimeter Quecksilbersäule) ist die Nachlast so gigantisch, dass ein vorgeschädigtes Herz das Blut nicht mehr auswerfen kann. Es kommt zum akuten Herzversagen und oft zum Lungenödem. Als Notfallsanitäter gibst du Vasodilatatoren (wie Urapidil), um die Blutgefäße zu weiten, die Nachlast drastisch zu senken und dem Herzen den Auswurf wieder zu ermöglichen.
3. Die Kontraktilität (Inotropie)
Die Kontraktilität beschreibt die reine, intrinsische Pumpkraft des Herzmuskels, völlig unabhängig von der aktuellen Vorlast oder Nachlast. Sie wird chemisch auf zellulärer Ebene gesteuert.
- Der Kalzium-Mechanismus: Die Stärke der Muskelkontraktion hängt direkt davon ab, wie viel Kalzium während der Systole in die Muskelzelle einströmt. Mehr Kalzium bedeutet, dass sich mehr Aktin- und Myosin-Fäden ineinander verhaken können, was zu einer explosiveren und kräftigeren Kontraktion führt.
- Sympathikus-Einfluss: Das vegetative Nervensystem steuert die Kontraktilität. Adrenalin und Noradrenalin binden an Beta-Rezeptoren am Herzen und öffnen zusätzliche Kalziumkanäle.
- Klinische Anwendung: Bei einem kardiogenen Schock (zum Beispiel nach einem massiven Herzinfarkt) ist totes Muskelgewebe nicht mehr in der Lage, sich zusammenzuziehen. Die globale Kontraktilität sinkt dramatisch. In diesem Fall verabreichst du positiv inotrope Medikamente (wie Adrenalin oder Dobutamin über einen Perfusor), um das noch lebende Muskelgewebe chemisch zu zwingen, sich maximal stark zusammenzuziehen und das Überleben zu sichern.
💡 MERKE:
Vorlast (Preload): Das Füllungsvolumen vor dem Schlag. Reguliert durch Volumeninfusion (steigert) oder Nitroglycerin (senkt). Nachlast (Afterload): Der Gefäßwiderstand beim Auswurf. Eine hohe Nachlast senkt das Schlagvolumen und erhöht den Sauerstoffbedarf massiv.Kontraktilität (Inotropie): Die reine, kalziumabhängige Muskelkraft. Wird durch Stresshormone (Adrenalin) gesteuert.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Blutdruckregulation (Mechanik und Neurologie)
1. Die Windkesselfunktion (Die mechanische Dämpfung)
Bevor das Nervensystem überhaupt eingreift, wird der Blutdruck rein physikalisch durch die Eigenschaften der Aorta (Hauptschlagader) und der großen herznahen Arterien reguliert. Diese großen Gefäße gehören zum elastischen Typ.
- Die systolische Dehnung: Wenn die linke Herzkammer in der Systole schlagartig etwa 70 Milliliter Blut auswirft, entsteht eine massive Druckwelle. Die stark elastische Wand der Aorta dehnt sich wie ein Luftballon aus, um dieses plötzliche Volumen aufzunehmen. Diese Dehnung dämpft die extreme Druckspitze ab (sie verhindert, dass der obere Blutdruckwert ins Unermessliche schießt). Gleichzeitig wird in der gedehnten Gefäßwand kinetische Energie gespeichert.
- Die diastolische Entladung: In der Diastole erschlafft das Herz, und die Aortenklappe schließt sich. Das Herz fördert in diesem Moment exakt 0 Milliliter Blut. Nun zieht sich die elastische Wand der Aorta automatisch wieder zusammen (wie ein Gummiband, das losgelassen wird). Durch dieses Zusammenziehen wird das gespeicherte Blut kontinuierlich weiter in den Kreislauf gepresst.
- Der biologische Sinn: Die Windkesselfunktion wandelt den stoßweisen, pulsierenden Auswurf des Herzens in einen gleichmäßigen, kontinuierlichen Blutstrom um. Ohne diesen Mechanismus würde der Blutdruck in der Diastole auf 0 Millimeter Quecksilbersäule abfallen, und der Blutfluss in den mikroskopischen Kapillaren käme völlig zum Erliegen.
2. Die Barorezeptoren (Die neurologischen Sensoren)
Zusätzlich zur Mechanik überwacht das vegetative Nervensystem den Blutdruck in Echtzeit durch hochspezialisierte Dehnungsrezeptoren (Barorezeptoren).
- Die strategischen Standorte: Diese Sensoren befinden sich primär an exakt 2 lebenswichtigen Orten: im Aortenbogen (Arcus aortae) und im Karotissinus (Sinus caroticus), einer leichten Erweiterung der inneren Halsschlagader. Diese Standorte sind genial gewählt, da sie den Druck des Blutes messen, das unmittelbar zum Gehirn und in den Körperkreislauf strömt.
- Das Messprinzip: Barorezeptoren messen keinen absoluten Druck, sondern die mechanische Dehnung der Gefäßwand. Je höher der Blutdruck, desto stärker wird das Gefäß gedehnt, und desto schneller feuern die Rezeptoren elektrische Aktionspotenziale ab.
- Die Datenleitung: Die Rezeptoren am Karotissinus senden ihre Signale über den Nervus glossopharyngeus (Hirnnerv 9) an das Gehirn. Die Rezeptoren im Aortenbogen nutzen den Nervus vagus (Hirnnerv 10). Das Zielgebiet ist das kardiovaskuläre Zentrum in der Medulla oblongata (verlängertes Mark).
3. Der Barorezeptorenreflex (Die Akut-Reaktion)
Das kardiovaskuläre Zentrum wertet die einströmenden Signale in Sekundenbruchteilen aus und steuert Herz und Gefäße über den Sympathikus und Parasympathikus entsprechend gegen.
- Reaktion auf Blutdruckabfall (Volumenmangel/Schock): Wenn der Blutdruck sinkt (zum Beispiel durch eine Blutung), werden die Gefäßwände weniger gedehnt. Die Barorezeptoren feuern weniger Signale ab. Das Gehirn registriert diesen Abfall und aktiviert massiv den Sympathikus, während der Parasympathikus gehemmt wird. Die Folge: Die Herzfrequenz steigt (Tachykardie), die Kontraktilität nimmt zu, und die peripheren Blutgefäße ziehen sich zusammen (Vasokonstriktion), um den Blutdruck wieder künstlich in die Höhe zu treiben.
- Reaktion auf Blutdruckanstieg (Krise): Steigt der Blutdruck massiv an, feuern die Rezeptoren wie wild. Das Gehirn reagiert, indem es den Sympathikus drosselt und den Parasympathikus über den Vagusnerv aktiviert. Die Herzfrequenz sinkt (Bradykardie), und die Blutgefäße weiten sich (Vasodilatation), um den Druck im Röhrensystem abzulassen.
💡 MERKE:
Die Windkesselfunktion der elastischen Aorta sorgt physikalisch dafür, dass das Blut auch in der Erholungsphase des Herzens kontinuierlich fließt. Barorezeptoren sind Dehnungssensoren im Aortenbogen und in der Halsschlagader. Bei einem Blutdruckabfall (Schock) greift der Reflex ein: Der Sympathikus wird aktiviert, das Herz rast und die Gefäße verengen sich, um das Überleben des Gehirns zu sichern.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Elektrophysiologie (Aktionspotenzial und EKG)
1. Das myokardiale Aktionspotenzial (Die Plateauphase)
Die Arbeitsmuskulatur des Herzens (Myokard) unterscheidet sich auf zellulärer Ebene massiv von deiner Skelettmuskulatur. Der entscheidende Unterschied liegt in der sogenannten Plateauphase, die das Herz vor einem tödlichen Dauerkrampf (Tetanus) schützt.
- Der schnelle Aufstrich (Depolarisation): Wie bei normalen Nervenzellen öffnen sich bei einem elektrischen Reiz zunächst spannungsgesteuerte Natriumkanäle. Positives Natrium schießt in die Zelle, und die elektrische Spannung schlägt extrem schnell in den positiven Bereich um.
- Die Plateauphase (Der Kalzium-Einstrom): Das ist die absolute Besonderheit des Herzens. Kurz nach dem Natrium-Einstrom öffnen sich spezielle, langsame Kalziumkanäle. Positives Kalzium strömt in die Zelle, während gleichzeitig etwas Kalium ausströmt. Diese beiden Ströme halten sich für etwa 200 bis 300 Millisekunden die Waage. Die Spannung bleibt auf einem hohen, positiven Plateau stehen. Dieser Kalzium-Einstrom ist gleichzeitig der Auslöser für die mechanische Muskelkontraktion (elektromechanische Kopplung).
- Die Repolarisation: Erst wenn sich die langsamen Kalziumkanäle wieder schließen, gewinnt der Kalium-Ausstrom die Oberhand. Die Zelle verliert positive Ladung, wird wieder negativ und kehrt in ihren Ruhezustand zurück.
- Die absolute Refraktärzeit: Durch dieses extrem lange Plateau ist die Herzmuskelzelle für fast die gesamte Dauer ihrer mechanischen Kontraktion absolut refraktär (unerregbar). Ein neuer elektrischer Reiz kann erst dann einen neuen Schlag auslösen, wenn der Muskel wieder komplett entspannt ist. Das macht ein lebensgefährliches "Verkrampfen" des Herzens rein physikalisch unmöglich.
2. Das Elektrokardiogramm (EKG)
Das EKG ist für den Notfallsanitäter das wichtigste diagnostische Werkzeug. Es zeichnet nicht die mechanische Kontraktion auf, sondern fängt die Summe aller elektrischen Ströme (Aktionspotenziale) ein, die wellenartig durch das Herz fließen.
- Die P-Welle: Sie ist die erste kleine, runde Welle im EKG. Sie repräsentiert die elektrische Erregungsausbreitung (Depolarisation) in den Vorhöfen, ausgehend vom Sinusknoten. Unmittelbar nach dieser elektrischen P-Welle kontrahieren die Vorhöfe mechanisch.
- Der QRS-Komplex: Dieser große, steile und schmale Ausschlag zeigt die schnelle und massive Erregungsausbreitung in den großen Herzkammern, vermittelt über das His-Bündel, die Tawara-Schenkel und die Purkinje-Fasern. Da die Kammern extrem viel Muskelmasse besitzen, ist dieser Ausschlag hoch. Die zeitgleiche Erregungsrückbildung der Vorhöfe geht in diesem massiven Komplex elektrisch völlig unter und ist im EKG nicht sichtbar.
- Die T-Welle: Diese letzte, breitere Welle zeigt die Erregungsrückbildung (Repolarisation) der Herzkammern. Die Zellen pumpen Ionen zurück und laden sich elektrisch wieder auf, um für den nächsten Herzschlag bereit zu sein.
💡 MERKE:
Das Aktionspotenzial des Herzens besitzt eine lange Plateauphase durch einströmendes Kalzium.Diese Phase erzeugt eine extrem lange Refraktärzeit, die das Herz vor einem Dauerkrampf schützt.Die P-Welle zeigt die elektrische Vorhoferregung.Der QRS-Komplex zeigt die massive Kammererregung.Die T-Welle zeigt die elektrische Kammererholung.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Hämodynamik und Kapillaraustausch
1. Die wahren Blutdruck-Parameter
Der Blutdruck ist viel mehr als nur ein oberer und ein unterer Wert auf dem Monitor. Die Organdurchblutung wird durch spezifische physikalische Drücke definiert.
- Der Pulsdruck (Pulse Pressure): Dies ist die reine mathematische Differenz zwischen dem systolischen und dem diastolischen Blutdruck. Bei einem Blutdruck von 120 zu 80 Millimeter Quecksilbersäule beträgt der Pulsdruck exakt 40 Millimeter Quecksilbersäule. Er repräsentiert die Auswurfkraft des Herzens und die Elastizität der Gefäße. Ein extrem enger Pulsdruck (zum Beispiel 90 zu 75) ist oft ein frühes Warnsignal für einen massiven Volumenmangel oder eine Herzbeuteltamponade.
- Mittlerer arterieller Druck (MAD / MAP): Dies ist der absolut wichtigste Parameter für dich im Einsatz. Der MAD ist der durchschnittliche Antriebsdruck, der das Blut durch das Gewebe presst. Da die Erholungsphase (Diastole) länger dauert als die Auswurfphase (Systole), ist der MAD nicht einfach der Mittelwert. Er berechnet sich aus dem diastolischen Druck plus 1 Drittel des Pulsdrucks. Ein MAD von mindestens 60 bis 65 Millimeter Quecksilbersäule ist zwingend erforderlich, um das Gehirn und die Nieren am Leben zu halten (Autoregulation).
2. Der Gefäßwiderstand (Die Physik des Blutflusses)
Das Blut fließt nicht ungehindert. Es reibt an den Gefäßwänden. Die Mathematik dahinter wird durch das Gesetz von Hagen-Poiseuille beschrieben. Der Widerstand wird von exakt 3 Faktoren bestimmt.
- Die Blutviskosität (Dicke): Je zähflüssiger das Blut ist (zum Beispiel bei massiver Exsikkose durch Flüssigkeitsmangel), desto schwerer lässt es sich pumpen.
- Die Gefäßlänge: Je länger das Röhrensystem, desto höher die Reibung. Bei erwachsenen Menschen ist dieser Wert jedoch relativ konstant und ändert sich nur bei extremer Gewichtszunahme (mehr Fettgewebe bedeutet längere Gefäßnetze).
- Der Gefäßradius (Der Hauptschalter): Dies ist der wichtigste Faktor! Der Radius geht in der physikalischen Formel in die 4 Potenz (hoch 4) ein. Das bedeutet: Wenn sich eine Arteriole durch die Gabe von Adrenalin auch nur minimal zusammenzieht und ihren Radius halbiert, steigt der Strömungswiderstand in diesem Gefäß sofort um das 16-fache an. Dein Körper nutzt diese winzigen Radiusänderungen, um den Blutdruck in Sekundenbruchteilen massiv zu manipulieren.
3. Der Kapillaraustausch (Filtration und Reabsorption)
Wenn das Blut in den mikroskopischen Kapillaren ankommt, muss die Flüssigkeit (das Blutplasma) mit den Nährstoffen durch die dünne Gefäßwand in das Gewebe gelangen. Dies geschieht durch einen ständigen Kampf von 2 gegensätzlichen Kräften (den sogenannten Starling-Kräften).
- Der hydrostatische Druck (Das Auspressen): Das ist der eigentliche Blutdruck in der Kapillare. Er wird vom Herzen erzeugt und presst das flüssige Blutplasma am arteriellen Anfang der Kapillare mit Gewalt durch die Poren der Gefäßwand nach außen in das Gewebe (Filtration). Rote Blutkörperchen und große Proteine passen nicht durch die Poren und bleiben im Blutgefäß zurück.
- Der kolloidosmotische Druck (Der Rücksog): Da die großen Proteine (vor allem Albumin) das Gefäß nicht verlassen konnten, sind sie am venösen Ende der Kapillare nun extrem hoch konzentriert, weil das Wasser ja ausgepresst wurde. Diese Proteine wirken wie physikalische Schwämme. Sie erzeugen einen osmotischen Sog, der das Wasser aus dem Gewebe wieder in die Kapillare zurückzieht (Reabsorption).
- Die Lymphgefäße (Der Überlauf): Es wird immer minimal mehr Wasser in das Gewebe gepresst, als durch die Proteine zurückgesaugt wird. Diese restliche Flüssigkeit (etwa 3 Liter pro Tag) wird vom Lymphsystem aufgesammelt und später wieder in die Venen geleitet.
💡 MERKE:
Der MAD (Mittlerer arterieller Druck) ist der wichtigste Wert für das Organüberleben (Minimum 60 Millimeter Quecksilbersäule).Der Gefäßradius ist der stärkste Hebel des Körpers: Eine Halbierung des Radius ver-16-facht den Widerstand. Der hydrostatische Druck presst Wasser in das Gewebe, der kolloidosmotische Druck (Proteine) saugt es wieder zurück in das Gefäß.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Regulation von Blutdruck und Durchblutung
Die Steuerung des Blutdrucks erfolgt gestaffelt: Das Nervensystem reagiert in Bruchteilen von Sekunden (Sofortregulation), die Hormone greifen nach Minuten bis Stunden ein (mittelfristige und langfristige Regulation), und die Autoregulation sichert das Überleben auf der lokalen Gewebeebene.
1. Die neuronale Kontrolle (Chemorezeptoren)
Neben den Barorezeptoren, die rein mechanisch den Druck messen, besitzt das Gefäßsystem chemische Überwachungssensoren.
- Die Sensoren: Chemorezeptoren sitzen ebenfalls strategisch im Aortenbogen und in der Halsschlagader. Sie messen kontinuierlich exakt 3 Parameter im Blut: den Sauerstoffgehalt, den Kohlendioxidgehalt und den pH-Wert (Säuregrad).
- Der Alarmzustand: Fällt der Sauerstoff ab oder steigen Kohlendioxid und Säuregrad (was auf einen Schockzustand oder Atemstillstand hindeutet), schlagen diese Rezeptoren sofort Alarm beim Gehirn.
- Die Reaktion: Das kardiovaskuläre Zentrum in der Medulla oblongata feuert über den Sympathikus. Die Herzfrequenz und die Herzkraft steigen massiv an, und die Blutgefäße ziehen sich zusammen (Vasokonstriktion), um das stark gefährdete Gehirn mit frischem Blut zu "spülen".
2. Die hormonelle Kontrolle (Das chemische Netzwerk)
Wenn der Blutdruck dauerhaft stabilisiert werden muss, greift der Körper auf hochpotente hormonelle Kaskaden zurück.
- Das RAAS (Renin-Angiotensin-Aldosteron-System): Dies ist das mächtigste System zur Blutdrucksteigerung. Fällt der Blutdruck ab, registrieren die Nieren das und schütten das Enzym Renin aus. Renin wandelt ein Bluteiweiß in Angiotensin I um. In der Lunge wird dieses durch das Angiotensin-Converting-Enzyme (ACE) in das hochaktive Angiotensin II umgewandelt. Angiotensin II ist einer der stärksten bekannten Vasokonstriktoren (verengt Blutgefäße massiv). Zusätzlich zwingt es die Nebennierenrinde, das Hormon Aldosteron auszuschütten, welches die Nieren anweist, Natrium und Wasser im Körper zurückzuhalten. Das Blutvolumen steigt.
- Das ADH (Antidiuretisches Hormon / Vasopressin): Dieses Hormon wird vom Hypothalamus gebildet. Bei einem massiven Volumenverlust (Blutung) wird es ausgeschüttet und befiehlt den Nieren, sofort die Wasserausscheidung (Urinproduktion) zu stoppen. Reines Wasser wird ins Blut zurückgeholt, um das Volumen zu retten. In hohen Dosen verengt es zudem die Blutgefäße.
- Das ANP (Atriales natriuretisches Peptid): Das ist der wichtigste Gegenspieler (Blutdrucksenker). Wenn das Blutvolumen zu hoch ist und die Vorhöfe des Herzens dadurch extrem stark gedehnt werden, schüttet der Herzmuskel selbst ANP aus. Es befiehlt den Nieren, sofort massenhaft Natrium und Wasser über den Urin auszuscheiden. Das Blutvolumen sinkt, der Blutdruck fällt.
3. Die Autoregulation (Die lokale Selbstbestimmung)
Das Faszinierende am Gefäßsystem ist, dass die einzelnen Organe nicht blind den Befehlen des Gehirns folgen. Sie können ihre Durchblutung an den präkapillaren Sphinktern selbst steuern.
- Metabolische Steuerung: Wenn ein Muskel plötzlich schwer arbeitet, verbraucht er Sauerstoff und produziert Milchsäure sowie Kohlendioxid. Diese Abfallstoffe wirken direkt auf die winzigen Muskeln der lokalen Blutgefäße und zwingen sie, sich weit zu öffnen (Vasodilatation). Das Gewebe holt sich genau das Blut, das es braucht.
- Stickstoffmonoxid (NO): Die innere Zellschicht der Blutgefäße (Endothel) kann als Reaktion auf Stress und chemische Reize das Gas Stickstoffmonoxid freisetzen. NO ist ein extrem potenter, lokaler Vasodilatator. Medikamente wie Nitroglycerin, die du beim Herzinfarkt gibst, funktionieren genau so: Sie setzen künstlich riesige Mengen an NO frei, um die Herzkranzgefäße gewaltsam zu weiten.
💡 MERKE:
Chemorezeptoren messen Sauerstoff und Säure; bei Mangel feuern sie den Sympathikus an. Das RAAS steigert Blutdruck und Blutvolumen durch Gefäßverengung und Wasserrückhalt. ADH stoppt die Urinproduktion bei Volumenmangel. ANP wird bei Überdehnung des Herzens ausgeschüttet und senkt das Blutvolumen. Autoregulation und NO erlauben es dem Gewebe, Gefäße lokal völlig selbstständig zu weiten.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
_____________________________________________________________________________________
Einleitung: Spezielle Kreisläufe (Ausnahmen der Hämodynamik)
1. Das Pfortadersystem der Leber (Die chemische Firewall)
Das Verdauungssystem hat die Aufgabe, Nährstoffe, aber potenziell auch Giftstoffe, aus der Nahrung in das Blut aufzunehmen. Wenn dieses Blut direkt in den Körperkreislauf (und damit zum Gehirn) fließen würde, wäre das lebensgefährlich.
- Der venöse Umweg: Das venöse, nährstoffreiche Blut aus Magen, Dünndarm, Dickdarm und Milz fließt nicht direkt in die untere Hohlvene. Stattdessen sammelt es sich in einem großen Sammelgefäß – der Pfortader (Vena portae hepatis).
- Das zweite Kapillarbett: Die Pfortader transportiert dieses Blut direkt in die Leber. Dort verzweigt es sich erneut in ein zweites Kapillarbett (die Lebersinusoide). Die Leber arbeitet nun als gigantischer biochemischer Filter.
- Die Filterfunktion: Leberzellen entnehmen dem Blut überschüssigen Zucker (um ihn als Glykogen zu speichern), verarbeiten aufgenommene Medikamente und entgiften Substanzen wie Alkohol oder Ammoniak.
- Der First-Pass-Effekt: Erst nachdem das Blut diese chemische Firewall passiert hat, verlässt es die Leber über die Lebervenen und fließt zum Herzen. Für dich als Notfallsanitäter ist das essenziell: Eine Tablette, die der Patient schluckt, muss zwingend durch diese Leberpassage und wird dort oft zu einem großen Teil abgebaut, bevor sie überhaupt am eigentlichen Zielorgan wirken kann (der sogenannte First-Pass-Effekt).
2. Der fetale Kreislauf (Leben ohne Atmung)
Im Mutterleib ist die Lunge des Fötus kollabiert, mit Fruchtwasser gefüllt und absolut funktionslos. Das sauerstoffreiche Blut kommt stattdessen über die Nabelschnurvene (Vena umbilicalis) direkt von der Plazenta der Mutter. Da die Lunge nicht durchblutet werden muss (und aufgrund des hohen Widerstands auch kaum durchblutet werden kann), besitzt das fetale Herz exakt 3 lebensrettende Kurzschlüsse (Shunts), um die Organe zu umgehen.
- Kurzschluss 1 (Ductus venosus): Das sauerstoffreiche Blut aus der Nabelschnurvene umgeht die fetale Leber zu einem großen Teil über dieses kleine Gefäß und fließt direkt in die untere Hohlvene in Richtung Herz.
- Kurzschluss 2 (Foramen ovale): Dieses Loch befindet sich direkt in der Herzscheidewand zwischen dem rechten und dem linken Vorhof. Das frische Blut schießt vom rechten Vorhof direkt in den linken Vorhof. Es umgeht somit die rechte Kammer und den Lungenkreislauf fast vollständig.
- Kurzschluss 3 (Ductus arteriosus): Das wenige Blut, das dennoch in die rechte Kammer gelangt und in den Lungenstamm gepumpt wird, stößt auf den massiven Widerstand der kollabierten Lunge. Der Ductus arteriosus ist eine direkte Gefäßverbindung zwischen dem Lungenstamm und der Aorta. Das Blut nimmt diesen Weg des geringsten Widerstands und fließt an der Lunge vorbei direkt in den Körperkreislauf.
- Die Geburt: Wenn das Baby den allerersten Schrei tätigt, entfaltet sich die Lunge. Der Druck im Lungenkreislauf fällt dramatisch ab. Durch diese plötzliche mechanische Druckumkehr verschließen sich das Foramen ovale und der Ductus arteriosus innerhalb von Minuten bis Stunden, und der normale Kreislauf des Erwachsenen ist etabliert.
💡 MERKE:
Das Pfortadersystem zwingt das Blut aus dem Darm zuerst durch den Filter der Leber (First-Pass-Effekt).Das Foramen ovale (Vorhofseptum) und der Ductus arteriosus (Gefäßbrücke) leiten das Blut beim Fötus an der nicht funktionsfähigen Lunge vorbei. Der erste Atemzug bei der Geburt verschließt diese fetalen Shunts durch die plötzliche Druckänderung in der Lunge.
Literatur und Quellen für dieses Modul
- Betts, J. G., Young, K. A., Wise, J. A., Johnson, E., Poe, B., Kruse, D. H., Korol, O., Johnson, J. E., Womble, M., & DeSaix, P. (2022). Anatomy and Physiology (2. Auflage). OpenStax.
